

|
Σύντομη
βιογραφία της συγγραφέως |
Κριτικές του άρθρου |

ISSN: 2241-4681
Ημερομηνία έκδοσης: Αθήνα 23 Μαρτίου 2020
![]()
Εργασία στα Οικονομικά της Υγείας και
Χρηματοοικονομικό Μάνατζμεντ Υπηρεσιών Υγείας
Καρέλη Αικατερίνη
Δρ. Ξένος Παναγιώτης,
Καθηγητής Frederick University
Δρ. Χαραλάμπους Γεώργιος, Καθηγητής Frederick University
Δρ. Σκίτσου Αλεξάνδρα, Καθηγήτρια Frederick University
![]()
Study in Economy’s
Health and Financial Management of Health Services
Kareli. A
Dr. Xenos Panagiotis, Professor Frederick University
Dr. Charalampous George, Professor Frederick University
Dr. Skitsou Alexandra, Professor Frederick University
![]()
Abstract
The methodology of cost –
effectiveness analysis, of cost – utility analysis through the cost – benefit
analysis, are appropriate methods for benchmarking between two medical
interventions. In this study, the compensation’s decision has been made with
criterion the benefit of society, that includes also the financial stability of
the health system of our country.
It appears that the
comparative methods of financial evaluation that analyze the cost –
effectiveness relationships in the health sector, are based, apart from the
economic and on social – moral criteria, in their attempt to suggest ways to
contain health cost as it does with our work study.
![]()
Περίληψη
Η μεθοδολογία οικονομικής ανάλυσης του κόστους –
αποτελεσματικότητας, κόστους χρησιμότητας μέσω της ανάλυσης κόστους οφέλους,
είναι ενδεδειγμένες μέθοδοι για την συγκριτική επιλογή ανάμεσα σε δύο
παρεμβάσεις ιατρικές. Στη συγκεκριμένη μελέτη,
η λήψη απόφασης αποζημίωσης έγινε με κριτήριο την ωφέλεια της κοινωνίας, το οποίο περιλαμβάνει και την
οικονομική σταθερότητα του συστήματος υγείας της χώρας μας.
Διαφαίνεται ότι οι συγκριτικές μέθοδοι οικονομικής
αξιολόγησης που αναλύουν τις σχέσεις
κόστους αποτελεσματικότητας στον υγειονομικό τομέα, στηρίζονται, εκτός από τα οικονομικά
και σε κοινωνικά – ηθικά κριτήρια, στην προσπάθειά τους να υποδείξουν τρόπους
συγκράτησης υγειονομικών εξόδων, όπως συμβαίνει με την μελέτη της εργασίας μας.
![]()
Εισαγωγή
«Η εισαγωγή της οικονομικής αξιολόγησης στην υγεία οφείλεται κυρίως στην
συνειδητοποίηση ότι οι πόροι δεν είναι
ανεξάντλητοι. Σύμφωνα με τον μελετητή David Elly , οι ιατρικές παρεμβάσεις έχουν κόστος, οι
άνθρωποι δεν είναι πάμπλουτοι και οι προϋπολογισμοί των προγραμμάτων υγείας είναι περιορισμένοι. Έτσι, για κάθε
υπηρεσία υγείας 1 δολαρίου που καταναλώνεται πληρώνεται 1 δολάριο». 1
Από την ανάλυση που προηγήθηκε διαφαίνεται
ότι η κυρίαρχη θεραπεία σήμερα για τον καρκίνο του προστάτη είναι η παρακάτω: «μεταστατικός
καρκίνος προστάτη (μ+), ορμονικός αποκλεισμός –φαρμακευτικός Lhrh ανάλογα-συνθετικά πεπτίδια της
υποθαλαμικής Lhrh, όπως
:γοναδορελίνη, λεουπρορελίνη, αντιανδρογόνα: Mη στεροειδή βικαλουταμίδη, νιλουταμίδη, φλουταμίδη & τα
στεροειδή αντιανδρογόνα.
Συνδυαστικές
θεραπείες σε μεταστατικό καρκίνο προστάτη
- Πλήρης αποκλεισμός των ανδρογόνων
- Μη στεροειδής μονοθεραπεία αντι-ανδρογόνου
- Διακεκομμένη/συνεχής θεραπεία στέρησης ανδρογόνων
- Άμεση/αναβαλλόμενη θεραπεία στέρησης ανδρογόνων
- Στέρηση των ανδρογόνων σε συνδυασμό με άλλους παράγοντες
Ορμονικός αποκλεισμός-χειρουργικός (υποκάψια ορχεκτομή)
Μεταστατικός ευνουχοάντοχος καρκίνος προστάτη (δεν
καταστέλλεται από τον ορμονικό αποκλεισμό)
Θεραπεία πρώτης γραμμής:
- οξική
αμπιτατερόνη
- ενζαλουταμίδη
- δοσεταξέλη
( χημικοθεραπευτικό )
- sipuleucel-t( ανοσοθεραπευτικό )
- μεταστατικός
ευνουχοάντοχος καρκίνος προστάτη
(δεν καταστέλλεται από τον ορμονικό αποκλεισμό)
Θεραπεία δεύτερης γραμμής :
- Cabazitaxel (ΧΗΜΕΙΟΘΕΡΑΠΕΙΑ)
- Abiraterone acetate after prior docetaxel
- Enzalutamide after docetaxel
- Radium-223
Θεραπεία
κατά των οστικών μεταστάσεων
- Διφωσφονικά
·
RANK-LIGAND»2
Στο πεδίο της ανοσοθεραπείας τα αποτελέσματα είναι ενθαρρυντικά αλλά όχι βέβαια αυτή τη
στιγμή και αφορούν το μεταστατικό στάδιο της νόσου.
«Ο καρκίνος του προστάτη είναι μια σύνθετη νόσος ,
στην οποία θα πρέπει να λαμβάνονται υπόψη πολλές πλευρές σχετικά με τη νόσο
αυτή κάθε αυτή, καθώς και τον ασθενή , πριν ληφθούν αποφάσεις που αφορούν τη
διαγνωστική προσέγγιση , τη θεραπεία και την παρακολούθηση».3Από τη
χρησιμοποίηση των 2 μεθόδων οικονομικής ανάλυσης για τον καρκίνο του
προστάτη , της κυρίαρχης και της νέας θεραπείας- ανοσοθεραπείας,
υπερέχει η μεθοδολογία του κόστους αποτελέσματος , με κριτήριο το γεγονός «ότι κάθε απόφαση για
την υγεία έχει και άλλες οικονομικές και κοινωνικές επιδράσεις όχι μόνο στο
άτομο που κάνει χρήση της υπηρεσίας υγείας αλλά και σε όλο το κοινωνικό σύνολο.»4
Τα αποτελέσματα της μη αποζημίωσης της νέας θεραπείας
αφορούν τη δεδομένη χρονική περίοδο και λαμβάνονται υπόψη ιατρικά δευτερογενή αποτελέσματα.
Τα έξοδα που σχετίζονται με τον προστάτη κατά τους
πρώτους 6 μήνες μετά τη θεραπεία της
ριζικής προστατεκτομής ως κυρίαρχη ήταν 12,184 δολάρια , μετά από 6 μήνες το
μέσο ετήσιο κόστος ήταν 2418 δολάρια . Το ετήσιο κόστος είναι 6707 δολάρια από
τα χαμηλότερα μεταξύ των μεθόδων αρχικής θεραπείας.
«Καρκίνος προστάτη –Εντοπισμένος χωρίς
μεταστάσεις
( ΣΤΑΔΙΟ: T1-T2)
- Θεραπεία: θεραπεία ίασης - ριζική προστατεκτομή
(ανοικτή οπισθοηβική, λαπαροσκοπική, ρομποτική)
- Ακτινοθεραπεία
( εξωτερική ακτινοβολία)
- Βραχυθεραπεία
(lowdose-highdose)
Αναφέρονται και εναλλακτικές θεραπείες
όπως hifu, cryoablation…αλλά είναι ακόμα
πειραματικές
Καρκίνος προστάτη –τοπικά προχωρημένη νόσος
( ΣΤΑΔΙΟ Τ3Ν0Μ0, Τ3Ν+ΜΟ)
- Θεραπεία “ίασης”
- Νέο - επικουρικός ανδρογονικός
αποκλεισμός + ριζική προστατεκτομή
- Ριζική προστατεκτομή +
επικουρικός ανδρογονικός αποκλεισμός
- Βραχυθεραπεία
+ ακτινοβολία + ανδρογονικός αποκλεισμός»5
Ο κίνδυνος και η ηλικία σχετίζονται σημαντικά με
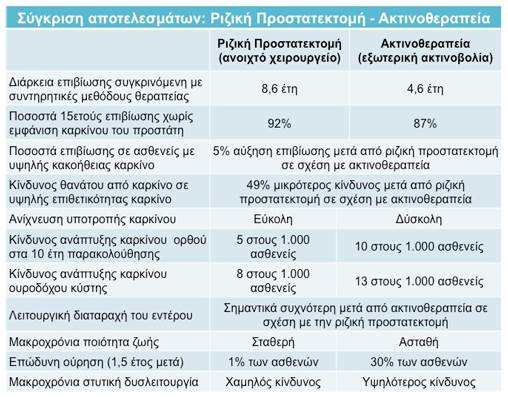
την αρχική επιλογή της θεραπείας. «Η ποιότητα ζωής είναι σταθερή στους άνδρες
ασθενείς που έχουν υποστεί ριζική προστατεκτομή» σύμφωνα με τους παρακάτω πίνακες 1,2.6
Πίνακας
1: Σύγκριση
αποτελεσμάτων μεταξύ ριζικής προστατεκτομής και ακτινοθεραπείας
http://www.poulakis-urology.com/da-vinci-ourologikes-epembaseis
Πίνακας
2 : Σύγκριση αποτελεσμάτων μεταξύ davinci και λαπαροσκοπικής
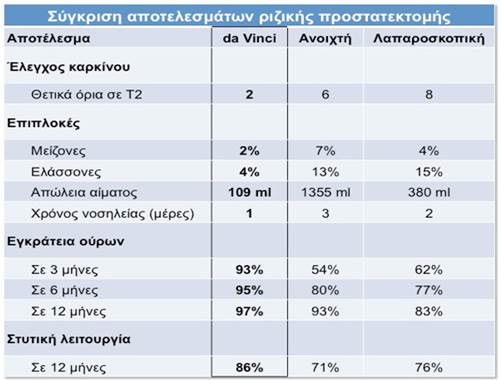
http://www.poulakis-urology.com/da-vinci-ourologikes-epembaseis
«Η εκτίμηση της αποτελεσματικότητας και
αποδοτικότητας της ανοσοθεραπείας σε πρώτη και δεύτερη κατηγορίας νέας
θεραπευτικής προσέγγισης, συντελείται δια μέσω χρησιμοποίησης της μεθοδολογίας της
οικονομικής ανάλυσης κόστους αποτελεσματικότητας, μεταξύ των υφιστάμενων θεραπειών
σε χρονικό πλαίσιο της σύγκρισης , το οποίο ισοδυναμεί με τα έτη ζωής
που προσδοκούν να ζήσουν οι άρρωστοι αυτοί.»1
«Το ΝICE θέτει ως
βασικό κατώφλι τις 30.000GBP/QALYή 33,624 .75 ευρώ αντίστοιχα προκειμένου να
θεωρηθεί μια παρέμβαση αποτελεσματική. Ωστόσο για τις θεραπείες στο τέλος της
ζωής, όπως αυτή που εξετάζουμε στην εργασία μας, οι επιτροπές αξιολόγησης του NICE προτείνουν θεραπείες με κόστος ανά QALYπάνω από το συνηθισμένο ανώτατο όριο των $ 30.000, κάπου γύρω στις $
50.000 . Με δεδομένο ότι οι $ 50.000 /QALY (56.110,43
Ευρώ) λαμβάνονται ως το κατώφλι για αυτές τις θεραπείες»1 , η νέα παρέμβαση
δεν γνωρίζουμε αν θα δύναται να επιλεχθεί
τη δεδομένη χρονική περίοδο. Για την κρίση των πιθανών αποτελεσμάτων που αφορούν την
ανοσοθεραπεία, δύναται να χρησιμοποιηθεί «ανάλυση ευαισθησίας».1
![]()
Κύριο μέρος
της εργασίας
(i)
«Η ανάλυση κόστους - αποτελεσματικότητας αποτελεί
τεχνική σύγκρισης του καθαρού χρηματικού
κόστους μιας θεραπευτικής παρέμβασης με κάποια μονάδα μέτρησης κλινικού αποτελέσματος
ή αποτελεσματικότητας, όπως είναι τα ποσοστά θνητότητας ή έτη ζωής».4
«Η μέθοδος ανάλυσης κόστους - αποτελεσματικότητας
επιτρέπει την αξιολόγηση επενδυτικών προγραμμάτων, εκτιμώντας το
κόστος σε χρηματικές μονάδες , ενώ τα οφέλη σε φυσικούς όρους και έτσι μετρούνται σε φυσικές μονάδες τα αποτελέσματα. Με τον τρόπο αυτό η
αποτελεσματικότητα εκφράζεται σε κόστος ανά μονάδα αποτελέσματος. Ο
δείκτης κόστους αποτελεσματικότητας (ΙCER- Incremental Cost - Effectiveness Ratio) μετρά το πρόσθετο κόστος που απαιτείται
για μια επιπλέον φυσική μονάδα αποτελέσματος
μετά από σύγκριση δύο θεραπευτικών μεθόδων».7
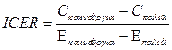
Στην
«μέθοδο της ανάλυσης κόστους χρησιμότητας - Ποιοτικά Προσαρμοσμένα έτη ζωής (QALY’S), η υγεία
θεωρείται κυρίως συνάρτηση δύο συντελεστών της διάρκειας ζωής και της ποιότητας
ζωής. Τα αποτελέσματα μιας ιατρικής
παρέμβασης μπορεί να εκτιμηθούν βάσει αυτών των διαστάσεων».7
«Η CUA μετρά το
κόστος της βελτίωσης /επιμήκυνσης της
ζωής και για την ανάλυση κόστους - χρησιμότητας μπορούν να
χρησιμοποιηθούν στοιχεία που αφορούν μόνο τελικές εκβάσεις (π.χ. κερδισμένες
ζωές) και όχι οι ενδιάμεσες εκροές (π.χ. αριθμός διαγνωστικών εξετάσεων ), που δεν προσφέρουν στην CUAδεδομένα που να μπορούν να εκφραστούν σε κάποια κατάλληλη μονάδα
μέτρησης».4
Τα
δεδομένα που αφορούν τον υπολογισμό του κόστους και της αποτελεσματικότητας ,
δεδομένου ότι «τα κόστη και τα οφέλη
επηρεάζουν τις ιατρικές αποφάσεις από
την πλευρά ενός φορέα χάραξης πολιτικής
υγείας , ο οποίος προσπαθεί να κάνει συνειδητές επιλογές όσον αφορά την
παραγωγή και την κατανομή των υπηρεσιών
ιατρικής περίθαλψης»4, προκύπτουν από την «ανάλυση του προσδιορισμού του κόστους , του «κόστους οφέλους» και της «αποδοτικότητας» 6
της νέας θεραπείας σε σχέση με την κυριαρχούσα θεραπεία του καρκίνου, του προστάτη προκειμένου
αυτά να ληφθούν υπόψη σύμφωνα με την έννοια της προεξόφλησης, την
νομισματική αξία της ζωής χρησιμοποιώντας μεθόδους , όπως το ανθρώπινο κεφάλαιο
και την επιθυμία του καταναλωτή να πληρώνει».6
«Το
συνολικό κόστος που επιβάλλεται σε μια
κοινωνία από την ιατρική πάθηση» εδώ του καρκίνου του προστάτη , περιλαμβάνει
«ως συνιστώσες
i.
τα
άμεσα κόστη ιατρικής περίθαλψης
ii.
τα
άμεσα κόστη μη ιατρικής περίθαλψης
iii.
τα
έμμεσα κόστη που αποτελούνται αρχικά από τα κόστη που συνδέονται με τον χρόνο
που απαιτείται για την εφαρμογή της θεραπείας
Ο αγοραστής υπηρεσιών υγείας, όπως εδώ το Υ.Υ. , προκειμένου
να αξιολογήσει «την εκτίμηση του
κόστους και την οπτική της ανάλυσής του»7 λειτουργεί «ως ερευνητής »7. «Όταν
ο ερευνητής επιχειρεί να συμπεριλάβει
όλες τις δυνατές συνέπειες αναφερόμαστε
στην κοινωνική προοπτική».8 «Αυτή
περιλαμβάνει τις εξής επιβαρύνσεις»
Πίνακας1: οπτική
της ανάλυσης και προσδιορισμός του κόστους
Πεδίο οπτικής της
ανάλυσης Προσδιορισμός κόστους (των
οικονομικών)
|
επιπτώσεων |
|
Κοινωνία Όλα τα είδη
ιατρικού και μη ιατρικού κόστους Απώλειες παραγωγής και
παραγωγικότητας Αόρατο κρυφό κόστος |
|
Κοινωνική Ασφάλιση ή Επιβαρύνσεις σχετικές με την αποζημίωση των προμηθευτών Ιδιωτική ασφάλιση |
|
Μονάδες Παροχής
Υπηρεσιών Υγείας Διάφορα είδη μεταβλητού κόστους, τα οποία επιδρούν στη δαπάνη περίθαλψης |
|
Ασθενής Όλα τα είδη
κόστους με έμφαση στις Ίδιες πληρωμές και την απώλεια παραγωγικότητας |
|
Εργοδότης-
Επιχείρηση Επιβαρύνσεις σχετικές με το κόστος
της ασφάλισης και την
απώλεια παραγωγικότητας |
Ανάλυση κόστους - αποτελεσματικότητας εναλλακτικών
πολιτικών για τον καρκίνο Τραχήλου, ως προς ένα από
τα «κύρια κριτήρια διάκρισης του Κόστους»8 σχετικά με «τον τρόπο
Ενσωμάτωσης των Στοιχείων αυτού στην παραγωγή»7.Με λίγα λόγια, «μπορεί να γίνει αυτοτελής
κοστολόγηση με την συμπερίληψη, στο κλινικό
Επίπεδο, και του κόστους των εργαστηριακών πράξεων ή άλλων παρεμβάσεων»8.
«Τα κύρια κριτήρια διάκρισης του κόστους που αφορά τον τρόπο διαμόρφωσης του
κατά τις μεταβολές του βαθμού απασχόλησης»8.
«Η εκτίμηση του κόστους μίας νόσου η οποία περιλαμβάνει
τα κάτωθι»8 :
Ø
«Άμεσο κόστος: το κατ’ εξοχήν κόστος που αναλώνεται
εξαιτίας της παρέμβασης .
Ø
To άμεσο Υγειονομικό
κόστος που προκύπτει από τους προμηθευτές υγείας (περιλαμβάνει το σύνολο των
δαπανών για την παρακολούθηση, τη θεραπεία, τις διαγνωστικές εξετάσεις, τα
φάρμακα κτλ ως αποτέλεσμα της θεραπείας).
Ø
Άμεσο
μη Υγειονομικό κόστος: oι
δαπάνες που ανακύπτουν για τον ασθενή ως αποτέλεσμα της νόσου αλλά και της
διαδικασίας αναζήτησης θεραπείας (δαπάνες βοήθειας στο σπίτι, δαπάνες
μετακίνησης, δαπάνες ειδικής διατροφής κ.ά)
Ø
Έμμεσο
κόστος :Οικονομικές απώλειες που ανακύπτουν ως αποτέλεσμα της νόσου χωρίς να
αφορούν στο κόστος παροχής της θεραπείας
Ø
Το
έμμεσο κόστος ουσιαστικά αναφέρεται στις απώλειες παραγωγικότητας εξαιτίας της
νόσου είτε λόγω απουσίας από την εργασία, είτε λόγω μειωμένης απόδοσης στην
εργασία
Ø
Αντανακλά
την αξία των αγαθών που θα μπορούσε να παράγει ο ασθενής εάν δεν είχε νοσήσει
Ø
Συνήθως
περιλαμβάνει τις απώλειες παραγωγικότητας, ελεύθερου χρόνου, χρόνου των
συγγενών οι οποίοι προστρέχουν προς
βοήθεια κ.ά.
Ø
Τέλος,
αυτό το είδος του κόστους συμπεριλαμβάνει και την απώλεια της παραγωγικότητας
λόγω του πρώιμου θανάτου του ασθενούς».8
Ø
Αόρατο
(ή άυλο) κόστος: όρος που περιγράφει τις δύσκολα μετρήσιμες επιπτώσεις της
νόσου και της θεραπείας
Ø
Οφείλεται
στο προκαλούμενο από το νόσημα ( ή τη θεραπεία) αισθήματα πόνου, δυσανεξίας,
υποβαθμισμένης ποιότητας ζωής ή άλλων κοινωνικών και ηθικών επιπτώσεων.
Ø
Στην
πράξη είναι δύσκολο να μετρηθεί ποσοτικά8
Πίνακας 4-5: Εκτίμηση του κόστους μιας
νόσου
|
Άμεσο Υγειονομικό Κόστος Άμεσο
μη Υγειονομικό Κόστος
Έμμεσο Κόστος Αόρατο Κόστος Θεραπευτικές
Μετακίνηση του ασθενούς Απώλεια ή μείωση
εισοδήματος Υποβάθμιση Ποιότητας
ζωής Παρεμβάσεις
από και προς νοσοκομεία οφειλόμενη σε
πρόσκαιρη, μερική ή μόνιμη αναπηρία
Κλινικές και ιατρεία Εργαστηριακές Μετακίνηση και διαμονή μελών της Απώλεια
εισοδήματος και μείωση παραγωγικότητας Κοινωνικά και Εξετάσεις οικογένειας
μελών της οικογένειας για τη φροντίδα κατ’ οίκο του ασθενούς επαγγελματικά
προβλήματα Ιατρικά Αγαθά Χρήση Διαγνωστικής Τεχνολογίας Ίδιες Πληρωμές
Διαταραχή οικογενειακής συνοχής Χρόνος Ιατρικού προσωπικού και άλλων από τον ασθενή Επαγγελματιών Υγείας Διαμονή
και εξυπηρέτηση
|
|
Ιατρικά Αγαθά |
Οικιακή βοήθεια και νοσηλευτική φροντίδα |
Απώλεια και μείωση της παραγωγικότητας
εργαζομένων και της παραγωγής των εργοδοτών και της κοινωνίας |
Δυσχερείς ψυχοκοινωνικές συνθήκες |
||
|
Χρήση Διαγνωστικής Τεχνολογίας |
Ίδιες πληρωμές από τον ασθενή |
Διαταραχή οικογενειακής συνοχής |
|||
|
Χρόνος Ιατρικού Προσωπικού και Άλλων Επαγγελματιών Υγείας |
|||||
|
Διαμονή και εξυπηρέτηση |
|||||
Πηγή:
(Αθανασιάδη Ε. 2015)
«Τα δεδομένα που απαιτούνται να
υπάρχουν στην οικονομετρική ανάλυση , όπου η πλέον συνηθισμένη μορφή κοστολόγησης των υπηρεσιών υγείας (C) που χρησιμοποιείται για μια θεραπεία ή για ένα πρόγραμμα
υγείας, βασίζεται στη γενικευμένη μαθηματική σχέση του κόστους όπου το κόστος
εκφράζεται ως συνάρτηση των εισροών , των τιμών και άλλων εξωγενών παραγόντων ,
όπως η τεχνολογία, το υγειονομικό σύστημα και άλλοι»9
Κόστος
= Εισροές, τιμές, τεχνολογία, υγειονομικό σύστημα
«Οι οικονομολόγοι υπολογίζουν
τις οικονομικές συνέπειες μιας νόσου ως το άθροισμα του αποδοτέου άμεσου και
έμμεσου κόστους»10
«Μια ανάλυση κόστους-αποτελεσματικότητας
έχει μεγαλύτερο ενδιαφέρον, όταν η νέα παρέμβαση είναι πιο αποτελεσματική και
κοστίζει περισσότερο από την υπάρχουσα παρέμβαση. Στις περισσότερες μελέτες
χρησιμοποιούνται οι παρακάτω δείκτες υγείας:
v Κλινικές
Μελέτες
v Δείκτες
Θνησιμότητας
v Δείκτες
Νοσηρότητας
v Δείκτες
Ποιότητας Ζωής»10
(ii) Αντιμετώπιση
«ΑΡΧΙΚΟ ΣΤΑΔΙΟ – ΕΝΤΟΠΙΣΜΕΝΟΣ ΚΑΡΚΙΝΟΣ
ΠΡΟΣΤΑΤΗ
Είδη θεραπείας:
Αναβαλλόμενη θεραπεία (ενεργής επαγρύπνηση/προσεκτική αναμονή)
Στην εντοπισμένη
ασθένεια, το προσδόκιμο ζωής τουλάχιστον 10 ετών θεωρείται υποχρεωτικό για κάθε
όφελος από την τοπική θεραπεία. Η συννοσηρότητα είναι πιο σημαντική από την
ηλικία στην πρόβλεψη του προσδόκιμου ζωής στους άνδρες με PCa (= καρκίνο του
προστάτη). Ωστόσο, για εκείνους τους άνδρες με σύντομο προσδόκιμο ζωής, η
προσεκτική αναμονή (WW) μαζί με θεραπεία καθοδηγούμενη από τα συμπτώματα είναι
κατάλληλη για τη διατήρηση της ποιότητας της ζωής.
Πολλοί άνδρες με εντοπισμένο καρκίνο του
προστάτη που διαγνώστηκε με προσυμπτωματικό έλεγχο δεν θα επωφεληθούν από
θεραπευτική αγωγή και το 45% αυτών είναι κατάλληλοι για ενεργή επαγρύπνηση. Η
θνησιμότητα σε ασθενείς με GS 5-7 που
δεν έχουν υποβληθεί σε θεραπεία για καρκίνο του προστάτη που ανιχνεύθηκε με
προσυμπτωματικό έλεγχο μπορεί να είναι τόσο χαμηλή όσο το 7% σε δεκαπέντε
χρόνια παρακολούθησης.
Υπάρχουν δύο διαφορετικές στρατηγικές για
τη συντηρητική διαχείριση που στοχεύουν στη μείωση της υπερβολικής θεραπείας: η
ενεργής επαγρύπνηση (AS) και η προσεκτική αναμονή (WW )».11
«Ορισμοί: Η ενεργής επαγρύπνηση στοχεύει στην
επίτευξη του σωστού χρόνου για την θεραπευτική αγωγή σε ασθενείς με κλινικά
εντοπισμένο καρκίνο του προστάτη, αντί για την καθυστερημένη παρηγορητική
θεραπεία. Οι ασθενείς παραμένουν υπό στενή παρακολούθηση και η θεραπευτική
αγωγή υποκινείται από προκαθορισμένα όρια ενδεικτικά ενδεχόμενης απειλητικής
για τη ζωή νόσου, που είναι ακόμη πιθανώς θεραπεύσιμα, λαμβάνοντας υπόψη το
προσδόκιμο ζωής στο άτομο.
Η προσεκτική αναμονή αναφέρεται στη
συντηρητική διαχείριση, μέχρι την ανάπτυξη τοπικής ή συστημικής εξέλιξης με
(επικείμενα) παράπονα που σχετίζονται με την ασθένεια. Οι ασθενείς στη συνέχεια
υποβάλλονται σε θεραπεία ανάλογα με τα συμπτώματά τους, προκειμένου να
διατηρηθεί η ποιότητα ζωής».12
Ριζική προστατεκτομή
(ΡΠ)
«Ο στόχος της ΡΠ από οποιαδήποτε προσέγγιση
πρέπει να είναι η εξάλειψη της νόσου, ενώ, όπου είναι δυνατόν, να διατηρείται η
δυνατότητα ελέγχου των σωματικών λειτουργιών
και η ικανότητα. Η αύξηση της συννοσηρότητας αυξάνει σημαντικά τον
κίνδυνο θανάτου από αιτίες που δεν σχετίζονται με τον καρκίνο του προστάτη.
Η
εκτίμηση του προσδόκιμου ζωής είναι πρωταρχικής σημασίας για την παροχή
συμβουλών σε έναν ασθενή σχετικά με τη χειρουργική επέμβαση. Τα κύρια
αποτελέσματα από τις πολυκεντρικές Τυχαιοποιημένες Ελεγχόμενες Δοκιμές (RCTs)
που εμπλέκουν την ΡΠ συνοψίζονται στον Πίνακα 6.
Πίνακας 6: Ογκολογικά αποτελέσματα ριζικής προστατεκτομής σε ασθένειες
που περιορίζονται σε όργανα σε RCTs
|
Μελέτη |
Ακρωνύμιο |
Πληθυσμός |
Έτος
θεραπείας |
Διάμεσος
FU (mo) |
Κατηγορία
Ρίσκου |
CSS
(%) |
|
Bill-Axelson,
etal. 2014 |
SPCG-4 |
Προ-PSA
εποχή |
1989-1999 |
160 |
Χαμηλό
ρίσκο Ενδιάμεσο
ρίσκο |
89.8 84.9 (στα
18 έτη) |
|
Wilt,
etal. 2017 |
PIVOT |
Τα
Πρώτα Χρόνια των δοκιμών του PSA |
1994-2002 |
152 |
Χαμηλό
ρίσκο Ενδιάμεσο
ρίσκο |
95.9 91.5 (στα
19.5 έτη) |
|
Hamdy,
etal. 2016 |
ProtecT |
Πληθυσμός
που εξετάστηκε |
1999-2009 |
120 |
Κυρίως
χαμηλό- και ενδιάμεσο ρίσκο |
99 (στα
10 έτη) |
CSS=επιβίωση ειδική/σχετική
με τον καρκίνο; FU=μεταπαρακολούθηση;
mo=μήνες; PSA=αντιγόνα σχετικά με τον
προστάτη; yr=έτος.»13,
14, 15
ΤΡΟΠΟΙ ΡΙΖΙΚΗΣ ΠΡΟΣΤΑΤΕΚΤΟΜΗΣ
- Χειρουργικές
τεχνικές
«Η προστατεκτομή μπορεί να πραγματοποιηθεί
με ανοικτές, λαπαροσκοπικές ή ρομποτικά υποβοηθούμενες προσεγγίσεις (RARP). Σε
μια τυχαιοποιημένη δοκιμή φάσης ΙΙΙ, η RARP αποδείχθηκε ότι είχε μειωμένους
χρόνους εισαγωγής και απώλεια αίματος αλλά όχι πρόωρες (δώδεκα εβδομάδες)
λειτουργικές ή ογκολογικές εκβάσεις. Η αυξημένη χειρουργική εμπειρία μείωσε
τους ρυθμούς επιπλοκών της ΡΠ και βελτιώθηκε η θεραπεία του καρκίνου. Τα
χαμηλότερα ποσοστά θετικών χειρουργικών περιθωρίων για τους χειρούργους μεγάλου
όγκου (μεγάλου αριθμού επεμβάσεων) υποδηλώνουν ότι η εμπειρία και η μεγάλη
προσοχή στις χειρουργικές λεπτομέρειες μπορούν να βελτιώσουν τον έλεγχο του
καρκίνου με ΡΠ. Υπάρχει έλλειψη μελετών που να συγκρίνουν τις διάφορες χειρουργικές
μεθόδους για αυτά τα μακροπρόθεσμα αποτελέσματα.»16, 17, 18, 19, 20
- Ακτινοβολία
«Εξωτερική Ακτινοθεραπεία Δέσμης (EBRT): Η Ακτινοθεραπεία Διαμορφούμενης
‘Έντασης (IMRT), με η
χωρίς την Ακτινοθεραπεία με Καθοδηγούμενη Εικόνα (IGRT), είναι ο χρυσός κανόνας για την EBRT.
Τεχνικές πτυχές: η ακτινοθεραπεία
διαμορφούμενης έντασης (IMRT)
και η ακτινοθεραπεία εξωτερικής δέσμης με ογκομετρικό τόξο (VMAT)
- Βραχυθεραπεία
1.Βραχυθεραπεία χαμηλής δόσης (LDR)
Η βραχυθεραπεία χαμηλής δόσης χρησιμοποιεί
ραδιενεργούς σπόρους που μόνιμα εμφυτεύονται στον προστάτη. Υπάρχει συναίνεση
σχετικά με τα ακόλουθα κριτήρια επιλεξιμότητας για τη μονοθεραπεία LDR: Στάδιο
cT1b-T2a N0, M0; GS 6 (βαθμός ISUP 1) με ≤ 50% πυρήνες βιοψίας που
εμπλέκονται με καρκίνο ή GS 7 (3 + 4), βαθμός ISUP 2) με ≤ 33% πυρήνες
βιοψίας που εμπλέκονται με καρκίνο. Ένα αρχικό επίπεδο PSA ≤ 10 ng / mL;
όγκος προστάτη <50 cm3, και μια Διεθνής Βαθμολογία για τα Συμπτώματα του
Προστάτη (IPSS) ≤ 12 και μέγιστη ταχύτητα ροής> 15 mL / min στις εξετάσεις
ροής ούρων.»21, 22
2. Βραχυθεραπεία υψηλής δόσης (HDR):
«Η βραχυθεραπεία υψηλής
δόσης χρησιμοποιεί μια ραδιενεργή πηγή που εισάγεται προσωρινά στον προστάτη
για να παράγει ακτινοβολία.
Θεραπεία:
Μεταστατικός καρκίνος του προστάτη
Εισαγωγή: Μια
Συστηματική Ανασκόπηση για την Θεραπεία Στέρησης Ανδρογόνων (ADT) στον Καρκίνο του Προστάτη έχει δημοσιευτεί
Ορμονική θεραπεία πρώτης γραμμής: Η
πρωτοβάθμια ADT υπήρξε το πρότυπο φροντίδας για πάνω από 50 χρόνια. Δεν
υπάρχουν στοιχεία επιπέδου 1 υπέρ ενός συγκεκριμένου τύπου ADT, ούτε για
ορχεκτομή ούτε για ανάλογο ή ανταγωνιστή LHRH. Η εξαίρεση είναι οι ασθενείς με
επικείμενη συμπίεση του νωτιαίου μυελού, για τους οποίους είτε οι αμφίπλευροι
ορχεκτομή, είτε οι ανταγωνιστές LHRH είναι οι προτιμώμενες επιλογές.»23
Συνδυαστικές
θεραπείες σε μεταστατικό καρκίνο του προστάτη
·
Πλήρης
αποκλεισμός των ανδρογόνων
- Μη στεροειδής μονοθεραπεία
αντι-ανδρογόνου
- Διακεκομμένη/συνεχής
θεραπεία στέρησης ανδρογόνων
- Άμεση/αναβαλλόμενη
θεραπεία στέρησης ανδρογόνων
- Στέρηση των
ανδρογόνων σε συνδυασμό με άλλους παράγοντες
- Συνδυασμός με οξική αμπιρατερόνη (abirateroneacetate): Σε δύο μεγάλες μελέτες RCT (STAMPEDE, LATITUDE)
μελετήθηκε η προσθήκη οξικής αμπιρατερόνης (1000 mg ημερησίως) συν Πρεδνιζόνης (5 mg ημερησίως) (ΑΑ συν P) σε ADT σε άνδρες με ευαίσθητο σε ορμόνες
μεταστατικό καρκίνο του προστάτη (mHSPC)»24, 25
ΑDT σε συνδυασμό με χημειοθεραπεία:
«Πραγματοποιήθηκαν
τρεις μεγάλες Τυχαιοποιημένες Ελεγχόμενες Δοκιμές (RCTs). Όλες οι
μελέτες σύγκριναν την ADT μόνη της ως πρότυπο φροντίδας με την ADT σε συνδυασμό
με άμεση δοκεταξέλη (docetaxel)
(75 mg /m2, κάθε τρεις εβδομάδες) (εντός τριών μηνών από την έναρξη της ADT). Ο
πρωταρχικός στόχος και στις τρεις μελέτες ήταν το OS.»26, 27, 28
Θεραπεία: Ευνουχοάντοχος
Καρκίνος Προστάτη (CRPC)
«Ορισμός του Ευνουχοάντοχου Καρκίνου Προστάτη: Ορός τεστοστερόνης
ευνουχισμού <50 ng / dL ή 1,7 nmol / L συν είτε · Ορός τεστοστερόνης
ευνουχισμού <50 ng / dL ή 1,7 nmol /
L συν είτε:
α, Μια βιοχημική εξέλιξη: Τρεις διαδοχικές
αυξήσεις του PSA κατά μία εβδομάδα, με αποτέλεσμα δύο αυξήσεις κατά 50% πάνω
από το ναδίρ, και ένα PSA> 2 ng / mL ή,
β. Ραδιολογική εξέλιξη: Η εμφάνιση νέων
βλαβών: είτε δύο ή περισσότερες νέες οστικές βλάβες στη σάρωση των οστών ή μια
αλλοίωση των μαλακών ιστών χρησιμοποιώντας RECIST (Κριτήρια Αξιολόγησης
Απάντησης σε Στερεούς Όγκους).»29
Θεραπεία πρώτης γραμμής για μεταστατικό
ευνουχοάντοχο καρκίνο του προστάτη (mCRPC)
«Η
αμπιρατερόνη αξιολογήθηκε σε 1.088 ασθενείς χωρίς χημειοθεραπεία, ασυμπτωματικούς
ή ελαφρώς συμπτωματικούς με mCRPC στη δοκιμή COU-AA-302 φάσης ΙΙΙ. Οι ασθενείς
τυχαιοποιήθηκαν σε οξική αμπιρατερόνη ή σε εικονικό φάρμακο, και τα δύο σε
συνδυασμό με πρεδνιζόνη. Στην τελική
ανάλυση με μέση παρακολούθηση 49,2 μηνών, το τελικό σημείο του OS ήταν
σημαντικά θετικό (34,7 έναντι 30,3 μήνες, HR: 0,81, 95% CI: 0,70-0,93, p =
0,0033).»30, 31
Ενζαλουταμίδη
(Enzalutamide)
«Μια τυχαιοποιημένη δοκιμή φάσης ΙΙΙ
(PREVAIL) περιελάμβανε έναν παρόμοιο πληθυσμό ασθενών και συγκρίθηκε η ενζαλουταμίδη
και το εικονικό φάρμακο. Η PREVAIL διεξήχθη σε πληθυσμό 1.700 ανδρών που δεν
είχε λάβει χημειοθεραπεία και έδειξε σημαντική βελτίωση και στα δύο συνοριακά
τελικά σημεία, rPFS (HR: 0,186, CI: 0,15-0,23, p <0,0001) και OS (HR: 0,706
· CI : 0,6-0,84, ρ <0,001). Μια μείωση ≥ 50% του PSA παρατηρήθηκε στο
78% των ασθενών. Τα πιο κοινά κλινικά σχετικά AEs ήταν η κόπωση και η υπέρταση. Η ενζαλουταμίδη ήταν εξίσου
αποτελεσματική και καλά ανεκτή στους άνδρες> 75 ετών καθώς και σε εκείνους
με ή χωρίς σπλαχνικές μεταστάσεις.»32, 33, 34
Δοσεταξέλη
(Docetaxel)
«Μια σημαντική βελτίωση
της μέσης επιβίωσης της τάξης των 2-2,9 μηνών παρατηρήθηκε με τη χημειοθεραπεία
με βάση τη δοσεταξέλη σε σύγκριση με τη θεραπεία με μιτοξαδρόνη (mitoxantrone) συν πρεδνιζόνη»35,
36
Sipuleucel-T (ανοσοθεραπευτικό φάρμακο).
«Το 2010, μια δοκιμή φάσης ΙΙΙ του
Sipuleucel-T έδειξε ένα όφελος επιβίωσης σε 512 ασυμπτωματικούς ή ελάχιστα
συμπτωματικούς ασθενείς με mCRPC. Μετά
από διάμεση παρακολούθηση 34 μηνών, η μέση επιβίωση ήταν 25,8 μήνες στην ομάδα
Sipuleucel-T σε σύγκριση με 21,7 μήνες στην ομάδα του εικονικού φαρμάκου, με HR
0,78 (p = 0,03). Δεν παρατηρήθηκε πτώση του PSA και η PFS ήταν παρόμοια και στα
δύο σκέλη. Η συνολική ανοχή ήταν πολύ καλή, με περισσότερες κυτταροκίνες που
σχετίζονται με AEs βαθμού 1-2 στην ομάδα
Sipuleucel-T, αλλά με την ίδια βαθμίδα 3-4 ΑΕs και στους δύο βραχίονες. Το Sipuleucel-T δεν είναι διαθέσιμο στην
Ευρώπη.»37
Θεραπεία
δεύτερης γραμμής για mCRPC
Καμπαζιταξέλη (Cabazitaxel)
«Η Καμπαζιταξέλη είναι
ένα νέο ταξάνιο με δραστικότητα σε καρκίνους ανθεκτικούς στη δοσεταξέλη.
Μελετήθηκε σε μια μεγάλη διερευνητική, τυχαιοποιημένη μελέτη φάσης ΙΙΙ (μελέτη
TROPIC) που συνέκρινε την καμπαζιταξέλη συν πρεδνιζόνη έναντι της μιτοξανδρόνης
συν πρεδνιζόνη σε 755 ασθενείς με mCRPC, οι οποίοι είχαν δείξει βελτίωση μετά ή
κατά τη διάρκεια χημειοθεραπείας με βάση τη δοσεταξέλη»38
Abiraterone acetate μετά την προηγούμενη docetaxel
- «Enzalutamide
μετά
docetaxel
- Radium-223 (Ράδιο-223)
Το Ράδιο-223 βελτίωσε σημαντικά το διάμεσο OS κατά 3,6 μήνες
(HR: 0,70 · p <0,001)»39
Πρόληψη
συμβάντων σχετικών με το σκελετικό
Διφωσφονικά
«Το ζολεδρονικό οξύ (zoledronicacid) έχει αξιολογηθεί σε mCRPC για τη μείωση
των σχετιζόμενων με το σκελετικό συμβάντων (SRE). Η μελέτη αυτή διεξήχθη όταν
δεν υπήρχαν διαθέσιμες δραστικές αντικαρκινικές θεραπείες εκτός από την
δοσεταξέλη. 643 ασθενείς που είχαν CRPC»40
Αναστολείς συνδέτη RANK (RANK ligand inhibitors)
Η
δενοσουμάμπη (denosumab) είναι ένα πλήρως ανθρώπινο μονοκλωνικό αντίσωμα που
στρέφεται ενάντια στο RANKL (ενεργοποιητής υποδοχέα του συνδέτη πυρηνικού
παράγοντα ΚΒ), ενός βασικού μεσολαβητή του σχηματισμού, λειτουργίας και
επιβίωσης των οστεοκλαστών. Στο M0 CRPC, η δενοσουμάμπη έχει συσχετιστεί με
αυξημένη επιβίωση χωρίς μεταστάσεις οστού σε σύγκριση με το εικονικό φάρμακο
(μέσος όρος ωφέλειας: 4,2 μήνες, HR: 0,85, p = 0,028).41
«Η ανοσοθεραπεία είναι η αξιοποίηση και ενίσχυση της φυσιολογικής
ικανότητας του ανοσοποιητικού μας συστήματος
να καταστήσει και πάλι τα καρκινικά κύτταρα ορατά διευκολύνοντας το ανοσοποιητικό
σύστημα να τα εντοπίσει και να τα καταστρέψει .Οι CAR ανοσοθεραπείες εφαρμόζονται μόνο σε ασθενείς που
απέτυχαν όλες οι άλλες θεραπευτικές προσεγγίσεις»42
Σύγκριση θεραπειών : Για τον εντοπισμένο καρκίνο του προστάτη η ολική
αφαίρεση του προστάτη με την ριζική
προστατεκτομή θεωρείται παραδοσιακά ο οριστικός τρόπος θεραπείας του καρκίνου. Τα
αρνητικά χειρουργικά όρια, είναι ένας πολύ καλός δείκτης ότι όλος ο καρκίνος
έχει πλήρως εξαιρεθεί.
Γράφημα 1 : Σύγκριση κινδύνου θανάτου
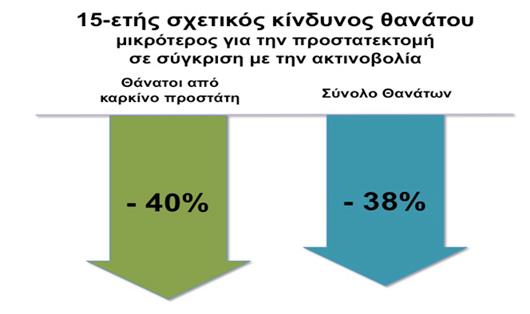
http://www.poulakis-urology.com/da-vinci-ourologikes-epembaseis
«Η περίοδος
επανόδου στην κανονική ζωή μετά την προστατεκτομή αφορά το 20ημερο , όπου οι περισσότεροι άνδρες
είναι έτοιμοι να γυρίσουν στις πρότερες ασχολίες και συνήθειες τους».3
Ανάλυση Κόστους
Στον καρκίνο του προστάτη «στο μεταστατικό στάδιο
υπάρχουν διάφορες ορμονοθεραπείες με
υψηλά κόστη».42 «Κυρίαρχη θεραπεία
στο αντίστοιχο στάδιο είναι αυτή της υποκάψιας ορχεκτομής σε σύγκριση με
το φαρμακευτικό ορμονικό ευνουχισμό στο
μεταστατικό καρκίνο του προστάτη ως νέα θεραπεία .Τα αποτελέσματα αυτής της μελέτης, εξηγούν με τη μελέτη
κόστους- αποτελεσματικότητας , δεδομένης της ανάγκης για μείωση του κόστους, αν
η ορχεκτομή αξίζει να εφαρμόζεται και αν δικαιολογείται ο μικρός αριθμός
επεμβάσεων στα πλαίσια των συστημάτων υγείας
της Ελλάδας και της Κύπρου. Μετά από
ανάλυση των πλεονεκτημάτων και μειονεκτημάτων της κάθε
μεθόδου ως προς τη συνολική επιβίωση, την ποιότητα ζωής, και τις ανεπιθύμητες
ενέργειες , μετρήθηκε το κόστος της
ορχεκτομής(Θεραπεία Α) και των
φαρμακευτικών θεραπειών(Θεραπεία Β) για
κάθε μήνα και για το σύνολο του χρόνου πιθανής επιβίωσης»42 .
«Τα αποτελέσματα έδειξαν ως συμπέρασμα ότι η
υποκάψια ορχεκτομή (Θεραπεία Α)είναι η θεραπεία με τον καλύτερο λόγο κόστους –
αποτελεσματικότητας. Τα ασφαλιστικά ταμεία στην Ελλάδα θα μπορούσαν να τη
χρησιμοποιήσουν έτσι ώστε να μειώσουν το κόστος τους.
Τρέχουσα
Θεραπεία Κόστος
(Α)
750 Ευρώ
(Β) 1868 Ευρώ για
διάστημα 30 μηνών με LHRH με το
φθηνότερο φάρμακο
Αποτυπώνεται
το κόστος της ορχεκτομής και των φαρμακευτικών θεραπειών για κάθε μήνα και για
το σύνολο του χρόνου πιθανής επιβίωσης»42.
Συμπέρασμα «Η
υποκάψια ορχεκτομή είναι η θεραπεία με τον καλύτερο λόγο κόστους-αποτελεσματικότητας».43
Θα πρέπει να αναφερθεί «ότι το κόστος
οποιασδήποτε ιατρικής διαδικασίας ή
τεχνολογίας είναι το ίδιο ανεξάρτητα από το αν εκτιμάται σε μια βάση κόστους –
αποτελεσματικότητας ή κόστους χρησιμότητας.Επίσης η ποιότητα ζωής που συνδέεται
με οποιαδήποτε ιατρική επιλογή παίζει ρόλο στο να αποφασιστεί η σχετική αξία
της».44
Στη μέθοδο της ανάλυσης κόστους αποτελεσματικότητας
«οι υπό εξέταση παρεμβάσεις ενδέχεται να
μειώνουν τις επιπτώσεις της νόσου, να εξαλείφουν τα συμπτώματα της ασθένειας,
να βελτιώνουν την ποιότητα ζωής των ασθενών, να επιμηκύνουν επίσης το
προσδόκιμο ζωής. Η διαφορά υπολογίζεται
από τη μέθοδο της εκλογής τη χρονική στιγμή εκπόνησης της ανάλυσης, δηλαδή την
παρέμβαση που εφαρμόζεται στην κλινική πράξη συνήθως για την αντιμετώπισή
της υπό εξέταση νόσου».44
Το ανωτέρω κόστος είναι «μεταβλητό»7,
«αποτιμάται περιοδικά και μεταβάλλεται χρονικά στο βαθμό της νέας τεχνολογίας
στην κλινική πράξη»7.
- «Το
μέτρο εκτίμησης της CEA είναι το αυξητικό όφελος που προκύπτει από μια παρέμβαση και το αντίστοιχο κόστος έναντι της θεραπείας που θεωρείται ως θεραπεία εκλογής και ο προσδιορισμός του λόγου της
διαφοράς τους»7 . Κατά την συγκεκριμένη συγκριτική
αξιολόγηση «έστω ότι οι δύο διαφορετικές θεραπείες Τ και S που συνδέονται με
συγκεκριμένο όφελος (Ε) και κόστος (C). Τα Ετ,Εs,Cτ, Cs συμβολίζουν το μέσο όφελος της νέας
θεραπείας, το μέσο όφελος της στάνταρ θεραπείας, το μέσο κόστος της νέας
θεραπείας και το μέσο κόστος της
στάνταρ θεραπείας, ενώ τα ΔΕ =Ετ-EskaiDC=Ct-Cs ορίζουν τις διαφορές του κόστους και
του οφέλους, αντίστοιχα.»7
Με
τη νέα θεραπεία παρατηρείται μια αύξηση της μέσης επιβίωσης και αντίστοιχη
αύξηση του συνολικού κόστους που συνοδεύει τη χορήγησή της, ως νεότερη
τεχνολογία υγείας που ενσωματώνει κόστος
έρευνας και τεχνολογίας. Το ερώτημα που πρέπει να απαντηθεί είναι το κατά πόσο
το παραπάνω κόστος δικαιολογείται από το επιπρόσθετο όφελος.
Γράφημα
2: διάγραμμα κόστους – αποτελεσματικότητας
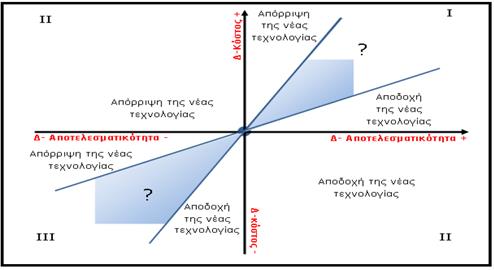
Πηγή:
Αθανασιάδη Ε 2015
«Ανάλυση κόστους
αποτελεσματικότητας και κόστους χρησιμότητας: Η αποτίμηση της
ποιότητας ζωής του ασθενούς επιχειρείται, προκειμένου να σταθμιστεί το
αποτέλεσμα μιας παρέμβασης σε σχέση με την ποιότητα της ζωής του ασθενούς. Ποιοτικά
σταθμισμένο έτος ζωής είναι ένα έτος. Η μέτρηση επιχειρείται με εξειδικευμένα
εργαλεία αποτύπωσης της εκτίμησης των ασθενών για την ποιότητα ζωής τους, όπως
το ΕQ-5D ο HealthUtilityIndex’»8 κτλ.
«Πολλοί
συμφωνούν ότι εάν η καινούργια ιατρική θεραπεία είναι λιγότερο από $50.000 για
κάθε επιπλέον έτος ζωής που αποκτιέται αυτό γενικά αντιμετωπίζεται ευνοϊκά».44
«Το ύψος του ICER είναι ο δείκτης που υπολογίζει το αυξητικό κόστος που απαιτείται ανά μονάδα οφέλους, για
παρεμβάσεις της ίδιας ασθένειας» «Έτσι έχει προταθεί να εξετάζεται η WTPτης κοινωνίας για ένα επιπλέον έτος ζωής».8
Γενικώς η
«φαρμακοοικονομία αξιολογεί την «ορθότερη»
κατανομή των πόρων , συγκρίνοντας
εναλλακτικές μεθόδους δράσης, με βάση τα κόστη και τα αποτελέσματά τους».8
Η επιλογή της θεραπείας με βάση τη σοβαρότητα της ψωρίασης και το οικονομικό
κόστος
Επιλογή
θεραπείας Κόστος Έτη ζωής που
κερδίζονται Δείκτης χρησιμότητας
υγείας QALY
Τρέχουσα Διαδικασία
Καινούργια Διαδικασία
(ανοσοθεραπεία (ενεργητική, παθητική,
επαγωγική)
«Το συνολικό μηνιαίο κόστος
θεραπείας για καρκίνο του
προστάτη σε αναδρομική μελέτη που έγινε από μια μεγάλη βάση δεδομένων των ΗΠΑ, που συνδέεται με εργαστηριακά δεδομένα» κατέδειξε
τα παρακάτω αποτελέσματα, αναφορικά με την «οικονομική επιβάρυνση και τη
χρησιμοποίηση της υγειονομικής περίθαλψης που σχετίζεται με τον ανθεκτικό στον
ευνουχισμό καρκίνο του προστάτη σε έναν εμπορικό πληθυσμό ασθενών και έναν
πληθυσμό Αμερικανών ασθενών με MedicareAdvantage”:»8
Πίνακα
7: συνολικό κόστος σχετικά με τον ανθεκτικό στον ευνουχισμό καρκίνο του
προστάτη στις ΗΠΑ
|
« |
Δείγμα πιθανών
ασθενών : |
Συνολικό κόστος
κατά Μ.Ο. |
|
|||||
|
349 με γνωστό CRPC |
2391 με πιθανό CRPC |
|
|
|||||
|
|
με βάση τα αποτελέσματα
PSA |
|
|
|||||
|
1,43
περιπατητικές επισκέψεις ανά ασθενή ανά μήνα |
1152 δολάρια (SD=$2073,sdείναι
η τυπική απόκλιση) |
1799 δολάρια και το κόστος αυτό αντιστοιχούσε
στο ήμισυ περίπου των δαπανών όλων των αιτιών υγειονομικής περίθαλψης για
αυτούς τους ασθενείς. |
|
|||||
|
Ο,4 διαμονής σε
νοσ/μείο ανά μήνα |
559 δολάρια για
παραμονή σε νοσοκομεία, 72 δολάρια για έξοδα φαρμακείου |
|
||||||
|
0,01 επισκέψεων
σε επείγοντα ανά μήνα |
1 δολάριο |
|
||||||
|
ΣΥΜΠΕΡΑΣΜΑ:OCRPC
είναι μία δαπανηρή ασθένεια, με
περιπατητικές επισκέψεις και ενδονοσοκομειακή περίθαλψη που αντιπροσωπεύουν
σημαντικό μέρος της οικονομικής επιβάρυνσης. Οι περιορισμοί που σχετίζονται
με τη χρήση δεδομένων αναδρομικών απαιτήσεων / διεκδικήσεων θα πρέπει να
λαμβάνονται υπόψη κατά την ερμηνεία αυτών των αποτελεσμάτων.» |
||||||||
Πηγή:
B.Alemayehuet. al 2010
«Σύγχρονα μοντέλα θεραπείας και αξιολόγησης του
καρκίνου του προστάτη αναγνωρίστηκαν χρησιμοποιώντας το CΑPSURE, ένα εθνικό
μητρώο νόσων των ανδρών με καρκίνο του προστάτη που περιελάμβανε συνεχή συλλογή
κλινικών δεδομένων από 31 ακαδημαϊκές και κοινοτικές ουρολογικές πρακτικές/ιατρεία
και τα αποτελέσματα από τα ανά διετία ερωτηματολόγια ασθενών, τα οποία
περιελάμβαναν τη δημογραφία, την ιατρική κατάσταση, την συννοσηρότητα, τα μέτρα
κινδύνου και τη χρήση της υγειονομικής περίθαλψης. Το κόστος των επισκέψεων
εξωτερικών ασθενών, των φαρμάκων και των νοσηλειών εφαρμόζονται/βρίσκονται από
διάφορες εθνικές πηγές. Η ανάλυση περιοδικών συμβάντων (MCF) αντιπροσώπευε την
αριστερή και τη δεξιά λογοκρισία. Ένα μοντέλο παλινδρόμησης μικτών επιδράσεων
με την μέθοδο bootstrappingγια
ασύμμετρα δεδομένα κόστους ποσοτικοποίησης τη σχέση μεταξύ κόστους MCF, ηλικίας
και κινδύνου.
Αποτελέσματα: Τα έξοδα που σχετίζονται με
το προστάτη κατά τους πρώτους 6 μήνες μετά τη θεραπεία ήταν 11.495 δολάρια, (από
2586 δολάρια για προσεκτική αναμονή/παρακολούθηση (WW–παρατηρείς στενά την
κατάσταση του ασθενή αλλά δεν δίνεις θεραπεία εκτός αν εμφανιστούν η
μεταβληθούν τα συμπτώματα) έως 24.204 δολάρια για ακτινοθεραπεία εξωτερικής
δέσμης. Μετά από 6 μήνες, το μέσο κόστος ήταν μόλις $3044. Το ετήσιο κόστος
είναι $7740, το υψηλότερο για θεραπεία στέρησης ανδρογόνων ($12.590) και το
χαμηλότερο για την προσεκτική παρακολούθηση ($5843). Ο κίνδυνος και η ηλικία
σχετίζονταν σημαντικά με την αρχική επιλογή της θεραπείας. Το αθροιστικό κόστος
(42.570 δολαρίων) επέτρεψε μια καλύτερη εκτίμηση του κόστους προτύπων
θεραπείας.
Συμπεράσματα: Το κόστος επιβάρυνσης του
καρκίνου του προστάτη είναι υψηλό, αλλά ποικίλλει ανάλογα με τον τύπο θεραπείας
ακόμα και όταν ελέγχεται για ασθένεια, ηλικία και στάδιο. Η αθροιστική ανάλυση
κόστους επέτρεψε τη συμπερίληψη των ανεπιθύμητων ενεργειών και των δαπανών
επανάληψης της νόσου, καθιστώντας εμφανείς νέες συγκρίσεις κόστους μεταξύ των
θεραπειών». 45
Πίνακας 8: Σύγκριση θεραπειών ριζικής
προστατεκτομής παλαιάς θεραπείας και τρέχουσας
|
Παλιά
θεραπεία |
Σύνολο
θεραπείας |
Μέσο
ετήσιο κόστος (MCF) |
ποσοστό
επιβίωσης |
ποσοστό
επιβίωσης σε επιθετικό καρκίνο |
|
1799
$ περιπατητικοί |
6
μήνες 11.495 |
42,570
$ |
92% |
5%
(μετά από ριζική προστατεκτομή) |
|
Ριζική
προστατεκτομή |
έτη
ζωής που κερδίζονται |
|
|
|
|
750 750 Ευρώ 1868
*30 μήνες 1-0 |
προσδίδονται 5 έτη επιπλέον *0,75=3,75 Αν λάΆν λάμβανε συγκεκριμένη 1 συγκεκριμένη
ιατρική διαδικασία .
Άρα η ιατρική διαδικασία δημιουργεί
3,75 QALY |
|
|
|
ΠΙΝΑΚΑΣ 9: «Κόστος
Θεραπείας σχετιζόμενη με τον Καρκίνο του Προστάτη κατά τύπο Θεραπείας, Ομάδα
Κινδύνου, Ηλικιακή Ομάδα και Εθνικότητα
|
|
Νο |
1ο 6μηνών μέσο όρο $/ασθενή |
Μέσο συνεχιζόμενο κόστος, $/6 μήνες |
Μέσο
ετήσιο κόστος, MCF$/περίοδο |
MCF, $ |
Στατιστικός z βαθμός |
Σημαντικότητα
με Bonferroni διόρθωση |
|
Αρχική
θεραπεία |
|
|
|
|
|
|
|
|
Ριζική προστατεκτομή |
2496 |
12,184 |
2418
|
6707
|
36,888 |
|
|
|
Κρυοθεραπεία |
135
|
7574
|
3270
|
7838
|
43,108 |
|
|
|
Βραχυθεραπεία |
668
|
7588
|
2635
|
6390
|
35,143 |
|
|
|
Ακτινοθεραπεία
εξωτερικής δέσμης |
409
|
24,204
|
3222
|
10,810
|
59,455 |
|
|
|
Στέρηση
ανδρογόνων |
607
|
8760
|
6019
|
12,590
|
69,244 |
|
|
|
Προσεκτική
παρακολούθηση |
238
|
2586
|
2947
|
5843
|
32,135 |
|
|
|
|
|
|
|
|
|
2.9281 |
<.05* |
|
D'Amico κλινικός
κίνδυνος |
|
|
|
|
|
|
|
|
Κίνδυνος
1 |
1829
|
10,826
|
2335
|
6108
|
33,593 |
|
|
|
Κίνδυνος
2 |
1454
|
11,676
|
2830
|
7251
|
39,882 |
|
|
|
Κίνδυνος
3 |
1018
|
12,736
|
4826
|
11,726
|
64,491 |
|
|
|
Όλοι
οι κίνδυνοι |
4553
|
11,495
|
2346
|
7740
|
42,570 |
|
|
|
|
|
|
|
|
|
2.6529 |
≤.05† |
|
Ηλικιακή
Ομάδα |
|
|
|
|
|
|
|
|
<55 |
483
|
12,656
|
2746
|
7199
|
39,594 |
|
|
|
55-65 |
1522
|
11,902
|
2655
|
7128
|
39,204 |
|
|
|
65-75 |
1812
|
11,587
|
3057
|
7972
|
43,848 |
|
|
|
>75 |
736
|
9664
|
4016
|
8829
|
48,560 |
|
|
|
|
|
|
|
|
|
2.6529 |
≤.05‡ |
|
Εθνικότητα |
|
|
|
|
|
|
|
|
Ιθαγενής
Αμερικανός |
11 |
19,261
|
7840
|
9818
|
53,999 |
|
|
|
Ασιάτης |
29 |
12,553
|
2246
|
5367
|
29,520 |
|
|
|
Ισπανός |
45 |
9151
|
2261
|
5788
|
31,833 |
|
|
|
Αφροαμερικανός |
218
|
10,689
|
3015
|
7396
|
40,678 |
|
|
|
Καυκάσιος |
3810
|
11,509
|
3059
|
7837
|
43,104 |
|
|
|
Μιγάς |
18 |
10,242
|
2648
|
6256
|
34,411 |
|
|
|
|
|
|
|
|
|
2.928 |
≤.05§ |
|
Όλοι
οι ασθενείς |
4553
|
11,495
|
3044
|
7740
|
42,570 |
|
|
Πηγή: Leslie S. et. al 2006
«Το MCF υποδεικνύει το μέσο αθροιστικό κόστος
λειτουργίας.
Όλα τα κόστη MCF για την πρωτογενή θεραπεία
διαφέρουν σημαντικά μεταξύ τους χρησιμοποιώντας το Ζ-τεστ και την κανονική
προσέγγιση με μεγάλους αριθμούς και με την πολύ συντηρητική προσαρμογή
Bonferroni, δηλ. κανένα από τα διαστήματα εμπιστοσύνης ήταν μηδέν, οπότε όλα
ήταν σημαντικά διαφορετικά μεταξύ τους
Όλα τα έξοδα MCF για τις ομάδες κινδύνου διαφέρουν
σημαντικά μεταξύ τους όταν χρησιμοποιούνται τα ίδια τεστ όπως παραπάνω.
Το κόστος όλων των ηλικιακών ομάδων MCF διαφέρει
σημαντικά μεταξύ τους ως ανωτέρω, με εξαίρεση τις ομάδες ηλικίας <55 έναντι
55-65 ετών που δεν διαφέρουν σημαντικά μεταξύ τους.
Το κόστος όλων των εθνοτήτων MCF διαφέρει σημαντικά
μεταξύ τους όταν χρησιμοποιούμε το Ζ-τεστ που περιγράφηκε παραπάνω, εκτός από
τους Ασιάτες που δεν διέφεραν από τους Αφροαμερικανούς ή τους Καυκάσιους, και
τους Ισπανούς και τους Αφροαμερικανούς, οι οποίοι δεν διέφεραν σημαντικά από
τους Καυκάσιους».45
Το μέσο κόστος της χημειοθεραπείας
«Η χημειοθεραπεία είναι μια χημική επεξεργασία που
βασίζεται για διάφορους τύπους καρκίνου που επιδιώκει να καταστρέψει τα
καρκινικά κύτταρα με τοξικές ουσίες χωρίς να βλάπτουν τον ασθενή. Οι τοξικές
ουσίες που χρησιμοποιούνται στη χημειοθεραπεία έχουν συνήθως αρνητικές και
μερικές φορές σοβαρά εξουθενωτικές συνέπειες για τις ασθενείς, αλλά ο στόχος
είναι πάντα να διατηρήσεις την υγεία του ασθενούς, μειώνοντας παράλληλα και την
εξάλειψη των καρκινικών στοιχείων από τον οργανισμό. Οι περισσότερες από τις
χημικές ουσίες που επιτίθενται και σε άλλα, υγιή κύτταρα του σώματος που είναι
παρόμοιες με τις ταχέως αναπτυσσόμενων καρκινικών κυττάρων, συμπεριλαμβανομένων
των κυττάρων των μαλλιών, η οποία είναι γιατί οι άνθρωποι που υποβάλλονται σε
χημειοθεραπεία χάνουν συνήθως τα μαλλιά τους. Πολλά ασφαλιστήρια συμβόλαια υγείας
περιλαμβάνει τουλάχιστον κάποιο είδος της κάλυψης για τη χημειοθεραπεία,
μειώνοντας σημαντικά το κόστος για τον ασθενή.
Το κόστος της χημειοθεραπείας δεν πρέπει να
μειώνεται σε φάρμακα μόνο. Δεδομένου ότι η θέση είναι επίσης ένας παράγοντας
στη τιμή, συγκοινωνιακούς φορείς ορισμένες φορές προσθέτουν δικά τους έξοδα, τα
οποία τα νοσοκομεία γενικά προσφέρουν στον ασθενή. Νοσήλια και τις χρεώσεις
υπηρεσιών που σχετίζονται με τη χορήγηση των φαρμάκων και της φροντίδας του
ασθενούς που χρειάζεται αργότερα θα πρέπει επίσης να υπολογιστούν, και αυτές
διαφέρουν από τόπο σε τόπο.
Δεδομένου ότι υπάρχουν πολλοί παράγοντες, το
πραγματικό κόστος της χημειοθεραπείας τείνει να ποικίλλει σημαντικά. Ωστόσο, οι
τιμές των παραδοσιακών φαρμάκων χημειοθεραπείας τείνουν να κυμαίνονται από 300$
έως 800$ για περίπου μια διάρκεια οκτώ εβδομάδων της θεραπείας, αν και μερικά
από τα πιο ασφαλισμένα φάρμακα μπορεί να είναι τόσο χαμηλό όπως 100$. Σύμφωνα
με τις πληροφορίες που απελευθερώνεται από το Εθνικό Ινστιτούτο Καρκίνου, τον Ιανουάριο
του 2009, 10 ετών αξίας των θεραπειών για τον καρκίνο του μαστού κοστίζουν κατά
μέσο όρο 21,000 ενώ του προστάτη και του καρκίνου του πνεύμονα κυμαίνονται γύρω
40,000$.
Οι μέσες τιμές των φαρμάκων δεν αντικατοπτρίζουν
πάντοτε το κόστος χημειοθεραπείας επειδή τα νέα φάρμακα αναπτύσσονται συνεχώς,
και αυτά κοστίζουν πολύ περισσότερο από ότι παλαιότερα, πιο κοινές
χημειοθεραπείες. Αυτά τα νεότερα φάρμακα, όπως η οξαλιπλατίνη και ιρινοτεκάνη,
μπορεί να κοστίσει 10,000$ ή περισσότερο.
Μέσο
κόστος χημειοθεραπείας
300
-800 $ για 8 εβδομάδες άρα 2 μήνες
100
$ με τα πιο ασφαλισμένα φάρμακα (φάρμακα μόνο)
10
ετών αξίας των θεραπειών του καρκίνου του προστάτη κυμαίνεται γύρω στα 40.000$
Για
πιο νέα φάρμακα χημειοθεραπείας 10.000$
για 1 πορεία θεραπείας (όπως η
οξαλιπλατίνη και ιρινοτεκάνη
10.000
$ ή περισσότερο για μια πορεία της θεραπείας , σύμφωνα με με το Chemotherapyfacts.com.
Τρέχουσα Διαδικασία θεραπείαςΑποτελεσματικότητα
(έτη ζωής που κερδήθηκαν) QALYΔείκτης
χρησιμότητας
300-800$ 10 έτη *0,75
7,5 75»46
Τρία νέα φάρμακα για τον Καρκίνο του
Προστάτη
«Το μόνο φάρμακο που έχει αποδειχθεί ότι
αυξάνει τις πιθανότητες επιβίωσης των ανδρών με καρκίνο του προστάτη ήταν το docetaxel, βασικό συστατικό του Lupron της AbbottLaboratories και είναι στη αγορά από το 2004.
Τα νέα εγκεκριμένα φάρμακα είναι για
περιπτώσεις που ο καρκίνος έχει εξαπλωθεί πέρα από τον αδένα του προστάτη. Το
ποσοστό επιβίωσης με τη χρήση του docetaxel ήταν περίπου 1,5 χρόνος. Τα νέα φάρμακα δίνουν ακόμα δύο με πέντε
μήνες, ενώ οι γιατροί δηλώνουν πως ο συνδυασμός φαρμάκων μπορεί να προσφέρει
τουλάχιστον δύο χρόνια.
Οι τιμές τους, όπως είναι αναμενώμενο,
είναι αρκετά υψηλές: το Provenge της Dendreon κοστίζει 93.000$ για έναν κύκλο θεραπείας, ενώ το Zytiga της Johnson&Johnson περίπου 5.000$ το μήνα. Ένα άλλο φάρμακο, το Jevtana της εταιρείας Sanofi, κοστίζει 8.000$ κάθε τρεις εβδομάδες.
Το πρόβλημα όμως είναι ότι το 80% των
ασθενών είναι στο πρόγραμμα υγείας Medicare, και με τις τιμές των φαρμάκων κάθε ασθενής θα χρειαστεί περίπου
500.000$ για μια ολοκληρωμένη θεραπεία, όπως αναφέρει ένας αναλυτής της
εταιρείας Lazard.
Η Medicare δήλωσε πως θα πληρώσει για Provenge μόνο όταν χρησιμοποιείται σύμφωνα με την εταιρεία και ισχυρίζεται πως
αυτό δεν έχει σχέση με την τιμή του. Το ίδιο κάνουν και οι ιδιωτικές εταιρείες
ασφάλισης για όλα τα φάρμακα.
Περίπου 280.000 άνδρες στις ΗΠΑ αποκτούν
καρκίνο του προστάτη κάθε χρόνο και περίπου 32.000 πεθαίνουν, σύμφωνα με την AmericanCancerSociety.
Τα νέα φάρμακα δημιουργήθηκαν για να
χρησιμοποιηθούν όταν, σε εξελιγμένες μορφές του καρκίνου, οι θεραπείες που
μειώνουν την παραγωγή τεστοστερόνης δεν είναι πλέον αποτελεσματικές.
Πολλοί γιατροί και ασθενείς υποστηρίζουν
τον ερχομό των φαρμάκων όπως το Zytiga
και το Provenge, γιατί
αντικαθιστούν τη χημειοθεραπεία, που μπορεί να έχει παρενέργειες.
Το Provenge «εκπαιδεύει» τον οργανισμό, ενώ το Zytiga, με την έκκριση ενός ενζύμου, ακινητοποιεί την
παραγωγή τεστοστερόνης.»47
Πίνακας 10: Μέσο κόστος χημειοθεραπείας
Τρέχουσα
Διαδικασία Θεραπείας
Τρέχουσα Διαδικασία Αποτελεσματικότητα (έτη ζωής που
κερδήθηκαν) QALYΔείκτης χρησιμότητας
300-800$ 10
έτη *0,75 7,5 75
Καινούργια Διαδικασία Κόιστος Έτη ζωής που
κερδίζονται Δείκτης χρησιμότητας
Φάρμακο 65.126 ευρώ
(93.000$) 2 έτη 1,5
5.600 ευρώ (8.000$)
Ανάλυση κόστους χρησιμότητας QALY
προεξόφληση αξίας ζωής
11.00$ για κάθε προσαρμοσμένη ποιότητα που 1,52 εκ. $ για άνδρες ηλικίας 20-24
ετών
Αποκτήθηκε
κατά τη διάρκεια της ζωής
10.000$ για κάθε qalyχειρουργείου
Ποσοστό
προεξόφλησης εξέτασης προεξοφλητική αξία αποδοχών
5%
τρέχουσα αξία αποδοχών ανδρών
1,06 εκ.$
Aξία ζωής
Αποδιδόμενη αξία ζωής
(με προσέγγιση ανθρώπινου κεφαλαίου) (με βούληση προς πληρωμή)
Προεξόφληση επιτοκίου3% 1,5
$ -2,5
20-24 ετών 1,52 εκ. $
εκ.$
(100$:1/10.000)
Αν ποσοστό 5%
20-24 ετών άνδρες
1,06 εκ. $
Cost(A)-Cost( B
) 93.000 -3.600 57.000ευρώ
---------------------- ------------------- = ----------------------
QALYS (A) -QALYS( B ) 7,5-1,5 6
«Από τον οριακό λόγο κόστους- αποτελέσματος
προκύπτει το ICER».8
To πηλίκο του λόγου κόστους αποτελεσματικότητας δεν πρέπει να υπερβαίνει
τις $ 50.000 . Από την ανάλυση που προηγήθηκε προκύπτει ότι το «ICER επικεντρώνεται όταν οι θεραπείες είναι ακριβότερες και
αποτελεσματικότερες»8. Για την εξαγωγή τελικών συμπερασμάτων,
οφείλει ένα τέτοιο κατώφλι του ICER
το οποίο θα αποτελέσει κριτήριο για εκείνες τις παρεμβάσεις που μεγιστοποιούν
την αποτελεσματικότητα.
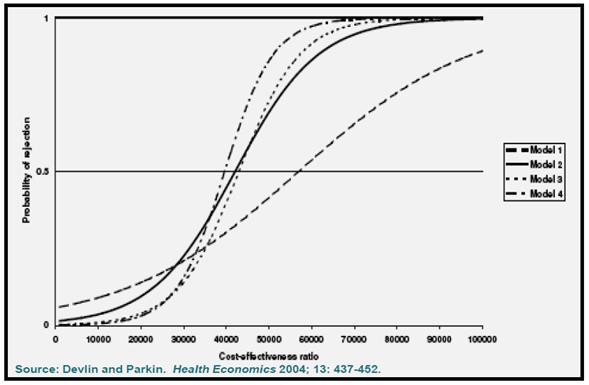
Γράφημα 8: Πιθανότητα
αποδοχής ανάλογα με το ύψος του ICER
Το συνολικό
αποτέλεσμα είναι ότι η αποδοχή της ανοσοθεραπείας ως σημαντικός παράγοντας για
την θεραπεία θα υπερβαρύνει το κόστος για το ΕΣΥ. Πιθανόν η ειδικότερη
υιοθέτηση ενός συνδυασμού φαρμάκου και εμβολίου στα πλαίσια της ανοσοθεραπείας να
βρίσκει έρεισμα για την χορήγηση και έγκρισή της σε ειδικές
ομάδες ασθενών ανδρών, όπου δίνεται έμφαση στις κοινωνικές πτυχές των Φορέων
Μ.Υ.
- Όσο
πιο επιθετικός είναι ο καρκίνος του προστάτη τόσο μεγαλύτερο είναι
το άμεσο και έμμεσο κόστος του
- Το κόστος εισαγωγής και εγχείρησης
είναι το πιο σπουδαίο κομμάτι των άμεσων κόστη
- Η ποιότητα ζωής του ασθενή επηρεάζεται
κατά πολύ
- Επιτακτικές οι σίγουρες θεραπείες που
προσφέρουν βέβαιο οριστικό αποτέλεσμα , όπως αυτό της ριζικής προστατεκτομής
ή της ορχεκτομής.
- Θα επιλεχθεί η θεραπεία της υποκάψιας ορχεκτομής ή της ριζικής
προστατεκτομής με τον καλύτερο λόγο κόστους αποτελεσματικότητας, σε
σύγκριση με αυτήν της ανοσοθεραπείας.
![]()
Επομένως με
βάση την σχηματική απεικόνιση του I.C.E.R
Συμπερασματικά, για κάθε θεραπευτική παρέμβαση,
προκειμένου να γίνει ο υπολογισμός του κόστους και της αποτελεσματικότητας , χρησιμοποιούμε την
ανάλυση κόστους οφέλους για την παλιά -κυριαρχούσα και τη νέα θεραπεία, που
πραγματοποιείται όταν το κοινωνικό όφελος «από αυτήν την παρέμβαση ξεπερνά το
κόστος της. Τα κόστη κάθε θεραπευτικής παρέμβασης υπολογίζονται με τον ίδιο
τρόπο όπως και στις δύο προηγούμενες αναλύσεις (κόστος αποτελεσματικότητας,
κόστος χρησιμότητας, αλλά και τα οφέλη / αποτελέσματος αποτιμώνται σε χρηματικές μονάδες ,
προκειμένου να συγκριθούν ευκολότερα με το αντίστοιχο κόστος του
θεραπευτικού προγράμματος. Η αποτίμηση
σε χρηματική αξία του οφέλους από τις θεραπευτικές παρεμβάσεις εκτιμώνται μέσω
δύο προσεγγίσεων. Η α΄ αφορά στην πρόθεση πληρωμής των ατόμων για τη
συγκεκριμένη παρέμβαση και η δεύτερη
αφορά στην προσέγγιση του ανθρώπινου κεφαλαίου
και στις συναλλαγές και περιλαμβάνει τις αποφάσεις που λαμβάνονται
ουσιαστικά. Σύμφωνα με τη διεθνή βιβλιογραφία τα οφέλη για την κοινωνία είναι η
υγεία, η παραγωγικότητα και η εξοικονόμηση μελλοντικών πόρων».10
Επίσης «γίνεται μια διάκριση της ανάλυσης κόστους –
αποτελεσματικότητας σε δυο μορφές: την ανάλυση κόστους αποτελεσματικότητας που δεν περιορίζεται από συγκεκριμένο μέγεθος
πόρων που πρέπει να δαπανηθούν για την υγεία, αλλά περιορίζεται από την αξία
που προσδίδει η κοινωνία στην κλινική πρακτική
και την οποία διατίθεται να πληρώσει για να βελτιώσει το υγειονομικό
αποτέλεσμα κατά ένα QALY. Η άλλη
μορφή είναι αυτή που δέχεται
περιορισμένους πόρους από τον προϋπολογισμό και καλείται να μεγιστοποιήσει την
αποτελεσματικότητα διατηρώντας χαμηλό το
κόστος μέσα στα όρια του προϋπολογισμού.
Επομένως η πρώτη
μορφή ανάλυσης μπορεί να φανεί περισσότερο ελκυστική στα στελέχη που
καλούνται να πάρουν αποφάσεις για την κατανομή των πόρων , καθώς στη δεύτερη
απαιτείται πλήρη γνώση του κόστους και αποτελεσματικότητας όλων των
υγειονομικών προγραμμάτων που υπάρχουν και χρηματοδοτούνται από τον
προϋπολογισμό. Αντίθετα στην πρώτη περίπτωση κάθε νέα θεραπευτική προσέγγιση
αξιολογείται με σύγκριση του πρόσθετου
κόστους και αποτελέσματος, χωρίς να λαμβάνεται υπόψη η κατανομή πόρων σε άλλα
υγειονομικά προγράμματα.
Τη δεδομένη χρονική στιγμή η
ανάλυση κόστους αποτελέσματος θα
επιλέγονταν με την α΄ μορφή διότι δεν δύναται να έχουμε πλήρη γνώση του κόστους
και της αποτελεσματικότητας για την ανοσοθεραπεία. Όταν τα πορίσματα για την
επιλογή ανάμεσα στις δυο υποκατηγορίες της ανάλυσης κόστους – αποτελεσματικότητας
είναι διαφορετικά καθώς οι προϋπολογισμοί
και οι επιλογές μεταβάλλονται , η επιλογή της καταλληλότερης μεθόδου συνδέεται
με τις επιλογές κατανομής πόρων σε όλους τους τομείς της κοινωνίας. Επειδή εδώ
«ο προϋπολογισμός είναι πλήρως ανελαστικός δεν επιλέγεται η β΄ υποκατηγορία Όταν
υπάρχει διαφορά ανάμεσα στην αξία που δίνει η κοινωνία σε μια κλινική παρέμβαση
και το ποσό του προϋπολογισμού που διατίθεται, αυτό μπορεί να υποδηλώνει την
ανάγκη για αναθεώρηση της αξίας αυτής ή αύξηση του διαθέσιμου προϋπολογισμού».4
«Επομένως, η οικονομική αξιολόγηση αφορά μόνο τη
νέα θεραπευτική προσέγγιση που εισάγεται , ενώ οι παλαιότερες δεν υφίστανται
αξιολόγηση. Ενδεδειγμένη η α’ υποκατηγορία που αναφέρθηκε διότι σύμφωνα
με τον μελετητή DONALDSON ταυτίζεται η
ανάλυση κόστους - αποτελεσματικότητας με
την α΄ υποκατηγορία , ενώ την ανάλυση κόστους – οφέλους με τη β΄ υποκατηγορία
και υποστηρίζει ότι δεν μπορούν να καταλήγουν σε ίδια πορίσματα.
Συμπερασματικά, σύμφωνα με τον JOHANNESSON «όταν η ανάλυση γίνεται από τη σκοπιά των
οικονομικών της ευημερίας ενδείκνυται η
ανάλυση κόστους οφέλους, ενώ όταν η ανάλυση
γίνεται ανεξάρτητα από τα οικονομικά της ευημερίας , ενδείκνυται η ανάλυση
κόστους αποτελεσματικότητας.»4
Για το λόγο ότι
δεν υπάρχουν συγκεκριμένα κόστη αποτελέσματος και κόστη οφέλους για την
ανοσοθεραπεία, «τα κόστη και τα οφέλη αυτής της ιατρικής απόφασης για τη νέα
θεραπεία, είναι δυνατό να προκύπτουν με την πάροδο του χρόνου παρά μία
συγκεκριμένη στιγμή.»7 με την
PV που σημαίνει
ότι ένα άτομο προτιμά 100$ σήμερα παρά σε ένα χρόνο από τώρα. Τα οριακά κόστη και τα οφέλη
της νέας θεραπείας που λαμβάνονται υπόψη συνδέονται με το σωστό επιτόκιο δηλ. 1
προεξοφλητικό επιτόκιο ανάμεσα στο 3-5%.
(iii) «Στην
διαδικασία λήψης αποφάσεων
στον τομέα της υγειονομικής
περίθαλψης »7, το κομμάτι όπου τα επιπλέον κόστη της
χορηγούμενης μεγαλύτερης ποσοτικά
ιατρικής φροντίδας είναι περισσότερα από τα οφέλη σε σχέση με την καλύτερη
παροχή φροντίδας υγείας «εξαρτάται από κάποιους παράγοντες, όπως η διαθεσιμότητα
των ιατρικών πόρων , οι προτιμήσεις των ασθενών και η βαρύτητα των ασθενειών».7
«Τα αποτελέσματα
από τη σύγκριση των 2 μεθόδων ανάλυσης , αφορούν «πολιτική σε
μακροεπίπεδο στην υγεία που σχετίζεται με τους μηχανισμούς που κάνουν
καταμερισμό των πόρων μέσα στο σύστημα υγείας ».4
«Πρέπει να συνδυαστεί η απόφαση για
κατανομή της δημόσιας δαπάνης σε
σχέση με την ιδιωτική, επιπλέον ότι οι φαρμακοβιομηχανίες έχουν διαφορετικές
επιδιώξεις , ότι οι ασφαλιστικοί οργανισμοί ασκούν πρόσθετες πιέσεις για κάλυψη
όλο και μεγαλύτερου πληθυσμού, ενώ η πολιτική υγείας πρέπει πάνω απ’ όλα να
παρέχει ίσες δυνατότητες στη χρήση των υπηρεσιών υγείας σε όλους».4
«Η ανάλυση
κόστους αποτελεσματικότητας στη μακροπολιτική χρησιμοποιείται για να
αξιολογήσεις νέες τεχνολογίες ή νέα φάρμακα που είναι έτοιμα να εισαχθούν στο
σύστημα υγείας».4Δεδομένου ότι η ανοσοθεραπεία βασίζεται σε λήψη
φαρμακευτικής αγωγής, «διαφορετική είναι η προσέγγιση της πολιτικής σε
μακροεπίπεδο στην υγεία ως προς την κοστολόγηση των φαρμάκων ανάλογα με το ποια
κόστη περιλαμβάνονται στη μελέτη».4
«Επειδή τα αποτελέσματα της οικονομικής
αξιολόγησης απαιτούν
συγκεκριμένη ανάλυση για την αξιολόγηση της σχέσης κόστους αποτελεσματικότητας, λόγω
του ότι η νέα ανοσοθεραπεία ταυτίζεται με βάση το στάδιο της ασθένειας του
καρκίνου του προστάτη, στη χορήγηση του συγκεκριμένου φαρμάκου, και καθόσον υπάρχει
περίπτωση να γίνει η χρήση του νέου φαρμάκου με την παράλληλη λήψη και άλλων
φαρμακευτικών σκευασμάτων ή εμβολίων, προκειμένου
να εκδοθούν συγκεκριμένες αποφάσεις για την κλινική αντιμετώπιση και την
αποζημίωση της νέας θεραπείας , με σκοπό την υπέρβαση του οφέλους (χρόνια ζωής) για χρήση συγκεκριμένων πόρων που υφίστανται, απαιτείται
πιθανόν βιβλιογραφική ανασκόπηση σε
τακτική βάση για την αποτελεσματικότητα και το κόστος.»1
Για τα συγκριτικά
αποτελέσματα θα πρέπει να «δημιουργείται
μητρώο με σκοπό τη συλλογή των κατάλληλων κλινικών αποτελεσμάτων,
οικονομικών δεδομένων για την υγεία και τη ποιότητα ζωής, το οποίο θα πρέπει να
αναθεωρείται περιοδικά και σε περιπτώσεις όπου ένα νέο φάρμακο καθίσταται
διαθέσιμο ή εμφανίζονται νέα στοιχεία για τα υπάρχοντα φάρμακα ή σε περιπτώσεις
αλλαγής των φαρμάκων».1
«Στην οικονομική αξιολόγηση της συγκεκριμένης
υπηρεσίας υγείας» θα εφαρμοστεί «ως σύγχρονη τεχνική οργάνωσης και
διαχείρισης η χρήση των DRGs:
§ Η λογική
είναι ότι οι περιπτώσεις , που εμφανίζουν ιατρικές – κλινικές αναλογίες και
προκαλούν παρόμοια αναλογική δαπάνη, εντάσσονται σε ομάδες και χρηματοδοτούνται
με τυποποιημένη αμοιβή.
§ Είναι
προφανές ότι η ένταξη σε Ομοιογενή Διαγνωστική Ομάδα συνεπάγεται ή υπονοεί την ακολούθηση
προτυποποιημένης κλινικής διαδρομής (πρωτοκόλλου) για την φροντίδα που θα
παρασχεθεί».7
«Με τα λογισμικά ομαδοποίησης -κύρια και
δευτερεύουσα διάγνωση , χειρουργικές και λοιπές επεμβάσεις, στοιχεία του
ασθενούς» για τον καρκίνο του προστάτη μπορούμε να αντλήσουμε οικονομικά
στοιχεία για τα κόστη και την αποτελεσματικότητα συγκριτικά των παλαιότερων
μεθόδων»7, την αξιολόγηση θεραπείας των αρρώστων και των νέων
μεθόδων ανοσοθεραπείας. Ειδικότερα
υπάρχουν “μεγάλες διαγνωστικές
κατηγορίες (25 ΜDSs) και για
τους ασθενείς του Ουροποιητικού Συστήματος ΜDC 117
Διάγραμμα 3: Διαγνωστικές κατηγορίες
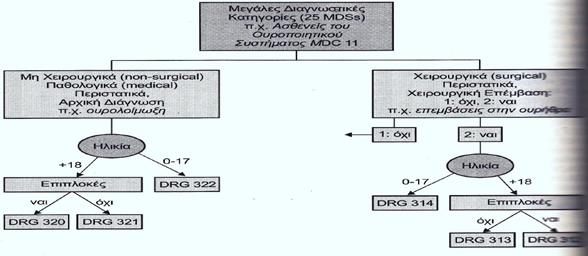
Πηγή: Μπαλασοπούλου2018
§
σύγχρονες
πολιτικές ελέγχου και συγκράτησης του κόστους των υπηρεσιών υγείας».7
§
«Μέσα
από την αντιστοίχιση των γνωστών παραδεκτών κλινικών διαδρομών και πληρωμών με
τα DRGs αναμένεται μια
μείωση ή τουλάχιστον συγκράτηση των δαπανών υγείας κυρίως λόγω της δυνατότητας
σύγκρισης και ελέγχου του κόστους».7
«Η αξιολόγηση
της αποτελεσματικότητας ενός μέτρου ιατρικού, εδώ της ιατρικής παρέμβασης της
μεθόδου της ανοσοθεραπείας, θεωρείται αποτελεσματικό σε ιατρικό επίπεδο, όταν επιφέρει θετικά
αποτελέσματα στην κατάσταση υγείας των
ανθρώπων και ενέχει πάντα ένα συγκρίσιμο
στοιχείο, το να είναι αποτελεσματικότερο από τα εναλλακτικά μέτρα που
λαμβάνονται για το ίδιο νόσημα».48 Τη δεδομένη στιγμή από τη
«συνδυασμένη αξιολόγηση και των 4 επιπέδων φροντίδας υγείας με την χρήση και
του επιπλέον παρακάτω δείκτη , αποτιμάμε
τη συγκεκριμένη θεραπεία , με συνδυασμό των οπτικών γωνιών των διαφορετικών
ομάδων που εμπλέκονται με την υγεία , όπως καταναλωτές, προμηθευτές, και
αγοραστές υπηρεσιών υγείας(ασφαλιστικοί
οργανισμοί) σύμφωνα και με τα βασικά κριτήρια της αποτελεσματικότητας,
αποδοτικότητας και ισότητας έως σήμερα.»48
«Σε πολλές χώρες
ακολουθείται μία τακτική ‘silo’
που σημαίνει ότι μελετώνται ξεχωριστά πόροι που απορροφώνται από συγκεκριμένες
δραστηριότητες στον τομέα υγείας(όπως ο φαρμακευτικός»4 σε σχέση με
τα νέα φάρμακα της ανοσοθεραπείας. Δηλαδή η τακτική ελάττωσης συγκεκριμένων ακριβών
φαρμακευτικών ιδιοσκευασμάτων ή εμβολίων, όπως εδώ της θεραπείας της ανοσοθεραπείας, ενδέχεται να
έχει ως αποτέλεσμα την υπερβολική χρήση άλλων θεραπειών φροντίδας υγείας με
ισότιμη ή μειωμένη αποτελεσματικότητα, οπότε γίνονται περισσότερες οι δαπάνες
υγείας στο σύνολό τους.
Αναφορικά με
την χρονική περίοδο της ανάλυσης «η
ηγεσία έρχεται αντιμέτωπη με αποφάσεις σχετικά με το αν θα πρέπει να
διοχετεύσει περισσότερους πόρους στην πρόληψη ή στην περίθαλψη, γεγονός που
εξαρτάται και από το σύστημα υγείας που δίνει στις μέρες μα ς έμφαση στην
πρόληψη σε σχέση με τη νοσοκομειακή
φροντίδα.»4
Στη
συγκεκριμένο είδος καρκίνου θα εφαρμοστεί και θα επιλεγεί η «μέθοδος
ανάλυσης κόστους – αποτελεσματικότητας ως κατάλληλης στην περίπτωση που τα
οφέλη εναλλακτικών προγραμμάτων είναι συγκρίσιμα, όπως εδώ, ή εφόσον έχει
προαποφασισθεί ότι συγκεκριμένα οφέλη πρέπει να παραχθούν, διότι μία ανάλυση
κόστους αποτελεσματικότητας έχει ενδιαφέρον όταν η νέα παρέμβαση είναι πιο
αποτελεσματική και κοστίζει περισσότερο από την υπάρχουσα».10
«Οι δείκτες
υγείας που χρησιμοποιούνται είναι των κλινικών μελετών, δείκτες
θνησιμότητας, δείκτες νοσηρότητας , δείκτες ποιότητας ζωής»10 από
τους οποίους προκύπτουν ασφαλή
συμπεράσματα για το κόστος και τα αποτελέσματα της θεραπευτικής παρέμβασης νέας
και κυρίαρχης των οποίων ο υπολογισμός γίνεται με βάση τον λόγο του διαφορετικού κόστους, προς το διαφορετικό
αποτέλεσμα.
Η αποτίμηση των αποτελεσμάτων αφορούν τους
ανωτέρω πίνακες αριθ. Σε «διάφορες
εκβάσεις υγείας, όπως η περίπτωση της ασθένειας του καρκίνου του προστάτη που
προλαμβάνεται»10 επιτυχώς με την ριζική προστατεκτομή και την
υποκάψια ορχεκτομή συγκριτικά «με το φαρμακευτικό ευνουχισμό και την
ανοσοθεραπεία στο μεταστατικό καρκίνο του προστάτη».43
Στην παρούσα
φάση «το όφελος που προκύπτει από τη ριζική προστατεκτομή και την υποκάψια
ορχεκτομή , είναι μεγαλύτερο από αυτό της ανοσοθεραπείας , η οποία είναι νέα
και δεν έχει χρησιμοποιηθεί ευρέως το φάρμακο αυτής στην Ελλάδα , άρα το
πρόσθετο όφελος αυτής δε δικαιολογεί το πρόσθετο κόστος και για το λόγο «αυτό
εγκαταλείπεται και δεν επιλέγεται έναντι των υπόλοιπων που κυριαρχούν αυτή την
στιγμή.43
Η «ανάλυση κόστους χρησιμότητας»10 δεν εφαρμόζεται συγκριτικά στην έρευνά μας,
διότι εκφράζει την προτίμηση . Στην ανάλυση κόστους χρησιμότητας ορίζεται ότι
τα έτη ζωής μπορεί να αποτιμηθούν και να αξιολογηθούν σύμφωνα με την ποιότητα
ζωής , Η μέτρηση της χρησιμότητας επιτυγχάνεται μέσω γενικών δεικτών όπως τα QALYs, τα Ποιοτικά Βελτιωμένα έτη ζωής και τα ισοδύναμα
έτη πλήρους υγείας ως μέτρο αποτελεσματικότητας.9
Στην έρευνα
μας για την « εκτίμηση της χρησιμότητας θα χρησιμοποιηθεί η τεχνική
του Χρονικού αντισταθμίσματος , όπου ο
ασθενής καλείται να επιλέξει την περίπτωση
της χρόνιας ασθένειας για το υπόλοιπο της ζωής του ή την περίπτωση της
κατάστασης της απόλυτης υγείας με μικρότερο όμως χρόνο ζωής».10
«Η απλούστερη μέθοδος μέτρησης της
χρησιμότητας αποτελεί η οπτική αναλογική κλίμακα, όπου ο ασθενής καλείται να
προσδιορίσει το επίπεδο υγείας του σε μια 100βαθμια κλίμακα.
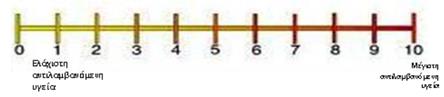
Γράφημα 9: Οπτική αναλογική κλίμακα
(visualanalogscale)
Με την μεθοδολογία
των QΑLY’s,
ως δείκτη που εξυπηρετεί των αξιολόγηση με βάση την έννοια της
ανακατανεμητικής
αποτελεσματικότητας « η
προσέγγιση στον καρκίνο του προστάτη θα
αφορά τις εξής περιπτώσεις :
1.
Η
διάθεση πόρων σε παρεμβάσεις που προσφέρουν περισσότερα QΑLΥ’s»8.
2.
«Hδιάθεση πόρων σε δύσκολες ασθένειες.»8
3.
«Την
διανομή των πόρων σε οριζόντια λαμβάνοντας υπόψη τον επιπολασμό»
4.
Την
επένδυση σε παρεμβάσεις πρόληψης με βάση τη χρόνια επίπτωση της νόσου στον
πληθυσμό.8
5.
Κοινωνικοί
και οικονομικοί παράγοντες διαδραματίζουν πιο σημαντικό ρόλο από ότι η ιατρική44
«Το ύψος του ICER ή
του λ με τον οποίο υπολογίζεται το αυξητικό κόστος που απαιτείται ανά μονάδα
οφέλους της παρέμβασης της ίδιας ασθένειας και αφορά τις περιπτώσεις όπου οι θεραπείες είναι ακριβότερες και
αποτελεσματικότερες»8 εφαρμόζεται και στη περίπτωση του καρκίνου του
προστάτη .
«Όλες ΟΙ παρεμβάσεις υγείας
μπορούν να καταταχθούν με ένα μέσο και να χρηματοδοτούνται εκείνες που έχουν το χαμηλότερο ΙCER.Για το λόγο αυτό η περισσότερο δαπανηρή θεραπεία
με την ανοσοθεραπεία για τον συγκεκριμένο καρκίνο του προστάτη, θα απορριφθεί
άνευ αποζημίωση με το «συνεπαγόμενο κοινωνικό κόστος αποκλεισμού.»8«Επίσης
τόσο η συνάρτηση παραγωγής όσο και ο προϋπολογισμός θεωρούνται σταθερά και
πλήρως γνωστά.»8
«Για τη λήψη απόφασης συνεπικουρεί όχι μόνον η οικονομική αξιολόγηση ως
εργαλείο, αλλά και η WTPt της κοινωνίας για
ένα επιπλέον έτος ζωής. «Αν είχε
προαποφασιστεί το WTP,
κάθε παρέμβαση με μικρότερο ΙCER θα αποζημιώνονταν».10
Ως
δεδομένο κρατάμε ότι «σύμφωνα με τον ΠΟΥ το επιθυμητό ύψος του δείκτη φτάνει περί του μέσου κατά κεφαλή
εισοδήματος της χώρας ,μια τιμή μικρότερη των 20.000 ευρώ θεωρείται ιδιαίτερα
ελκυστική ενώ άνω των 100.000ευρώ .8
Πίνακας 11:
Τιμές QALY ανά χώρα
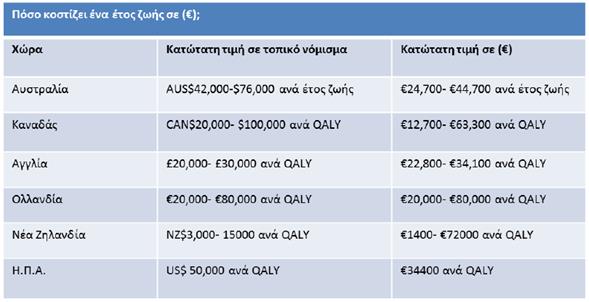
Πηγή: Αθανασιάδη 2015
Σύμφωνα με το αυστηρό κατώφλι ο δείκτης QALYsείναι καθοριστικό κριτήριο για τη διάχυση των πόρων
ενώ το ελαστικό ενσωματώνει και άλλες παραμέτρους προκειμένου να αποφασιστεί η αποδοχή του
προγράμματος».4 «Σύμφωνα με τον μελετητή Drummondτα κλινικά
αποτελέσματα θα συνοδεύουν τις αναλύσεις κόστους – αποτελεσματικότητας για την
υγεία πριν ληφθεί απόφαση για την κατανομή των πόρων ενώ η τιμή κατώφλι θα καθιερωθεί
στις αναλύσεις κόστους αποτελεσματικότητας για την υγεία»4
«Για την κατηγορία
του μεταστατικού καρκίνου του προστάτη η κυριαρχούσα θεραπεία είναι η
χειρουργική αντιμετώπιση με ασφαλή αποτελέσματα. Αντίθετα με την ανοσοθεραπεία
«που αποτελεί ένα από τα πιο σύγχρονα εργαλεία , που διαθέτει η επιστημονική
κοινότητα έναντι των νεοπλασιών , η κατανόηση των μηχανισμών και των
σηματοδοτικών μονοπατιών που βρίσκονται πίσω από το κατασταλμένο ανοσοποιητικό
σύστημα του οργανισμού, κατά τη διάρκεια του καρκίνου, έχει ήδη ξεκινήσει
και αναμένεται να κορυφωθεί μέσα στα επόμενα χρόνια (4).
Ο συνδυασμός των 2
χημειοθεραπευτικών προσεγγίσεων της Μετρονομικής χημειοθεραπείας και της
χημειοθεραπείας, μπορεί να διευρύνει το φάσμα των εφαρμογών των αντικαρκινικών φαρμάκων,
αυξάνοντας παράλληλα την αποτελεσματικότητα της θεραπείας. Συνδυασμός των δύο
ανωτέρω μεθόδων δείχνει ενίσχυση της αποτελεσματικότητας της ανοσοθεραπείας και
ανοίγοντας το δρόμο για το σχεδιασμό και την έγκριση φαρμακευτικών αγωγών με
αυξημένη και παρατεταμένη αποτελεσματικότητα αλλά με μειωμένη τοξικότητα.
Παρόλα αυτά η θέση της Μετρονομικής χημειοθεραπείας
από μόνη της ή σε συνδυασμό με την ανοσοθεραπεία στην καταπολέμηση του
καρκίνου, πρέπει να διερευνηθεί περαιτέρω». Συνδυασμός μετρονομικής χημειοθεραπείας
και ανοσοθεραπείας – θεωρητική και πειραματική προσέγγιση»49
«Την ποιότητα της οικονομικής ανάλυσης για τη λήψη
απόφασης την καθορίζουν και άλλοι παράγοντες»4, όπως :
1. «Η ανάγκη για περίθαλψη με βάση την ιατρική
απόδειξη που απορρέει κυρίως από τη δυσανάλογη αύξηση των υγειονομικών αναγκών
σε σχέση με την αύξηση των διαθέσιμων πόρων».4
2. Η γήρανση του πληθυσμού, η εισροή νέων τεχνολογιών
, οι αυξανόμενες προσδοκίες των ασθενών και οι αυξανόμενες προσδοκίες των
επαγγελματιών υγείας
3. Στον συνδυασμό εισροών που επιτυγχάνουν το μέγιστο
αποτέλεσμα με δεδομένο το κόστος παραγωγής(αρχή της διανεμητικής αποτελεσματικότητας)44
4. Το αναθεωρημένο πλαίσιο από τους Labelleet.al. ανάλυσης της δυνατότητας των γιατρών να προκαλούν
ζήτηση για τις υπηρεσίες τους44
5. Ο έλεγχος του κόστους και ποιότητας μέσω της ακριβούς κοστολόγησης (συλλογή
δεδομένων κλινικών και οικονομικών ως ενδεδειγμένη κλινική διαδρομή (κλινικά
πρωτόκολλα, ενσωμάτωση καινοτομίας, συνευθύνη ιατρών) «οι πυλώνες του DRGsystem».50
«Δεδομένου ότι στην οικονομική αξιολόγηση σκοπός δεν είναι
η ελαχιστοποίηση του κόστους, όσο η μείωση του ρυθμού αύξησης των
υπέρογκων δαπανών και φυσικά η ορθολογική χρήση των διαθέσιμων πόρων, εδώ το
κοινωνικό κόστους συνυπολογίζεται στην λήψη απόφασης και τα κριτήρια της
οικονομικής αξιολόγησης ενσωματώνουν τις απαιτήσεις για κοινωνική ευημερία».
Μελέτη κόστους – χρησιμότητας σε ασθενείς που έχουν υποβληθεί σε τοποθέτηση
οδοντικών εμφυτευμάτων».10
«Η περίοδος
ανάκτησης που είναι ένας χρυσός κανόνας που υποστηρίζει την αποδοχή ενός
επενδυτικού έργου, εφόσον αυτό επιστρέφει τις εκροές του μέσα σε μια
προκαθορισμένη χρονική περίοδο , η οποία μπορεί να προσαρμοστεί ώστε να
περιλάβει διάφορα στοιχεία, όπως το αρχικό κόστος επενδύσεων ή το κόστος συν ένα αποδεκτό
περιθώριο κέρδους. Επειδή επιλέγεται ως μέθοδος προσέγγισης στην αρχική εξέταση
της επενδυτικής πρότασης Όμως δεν διατίθεται ο μηχανισμός για να εξεταστούν τα
πιθανά έσοδα από μια επένδυση μετά το τέλος της περιόδου ανάκτησης και συνεπώς
τα αντιμετωπίζει ως απρόβλεπτα έσοδα. Μερικά εκλαϊκευμένα κριτήρια για τη
μέτρηση της απόδοσης διαφόρων επενδυτικών σχεδίων».1
«Οι
σημαντικές αποφάσεις που πρέπει να ληφθούν στο πλαίσιο ενός οργανωμένου
συστήματος υγείας αφορούν
§ κάλυψη (αποζημίωση του κόστους μιας
υγειονομικής παρέμβασης)» εδώ θεραπευτικής,
§
Στην ορθολογική και αποδοτική κατανομή των σπάνιων
πόρων. Ένα κατάλληλο εργαλείο για ορθολογική κατανομή των πόρων είναι η
οικονομική αξιολόγηση η οποία γίνεται με σκοπό να αποδείξει αν οι εξεταζόμενες
θεραπευτικές προσεγγίσεις δεν σπαταλούν πόρους υγείας». Στην τελική απόφαση
υπεισέρχονται και κοινωνικά και κριτήρια αξίας.»1
§
Σε κάποιες χώρες προαπαιτείται πριν την αποζημίωση
οικονομική αξιολόγηση των παρεμβάσεων.
§
Η ανάλυση που προηγήθηκε, «προσδιόρισε στην ουσία
την αποδοτικότητα της παρέμβασης και αποτελεί τη σχέση κόστους ευκαιρίας, όπου
το κόστος είναι η νομισματική αξία των χρησιμοποιούμενων εισροών για την
πραγματοποίηση μιας διαδικασίας και το ,όφελος όσο και τα αποτελέσματα είναι οι
εκροές. Δεδομένης της οικονομικής ύφεσης που διανύει η χώρα μας τα τελευταία
χρόνια , αλλά και των μνημονιακών υποχρεώσεων που επιβάλλουν συνεχή περιστολή
και των δαπανών για την υγεία, κρίνονται επιβεβλημένες οι οικονομικές
αξιολογήσεις των θεραπευτικών παρεμβάσεων προκειμένου να επιλέγονται εκείνες
που θα μεγιστοποιούν τα οφέλη για τον ασθενή με το λιγότερο δυνατό κόστος για
τον υγειονομικό τομέα.1
Συμπεράσματα: Στην ανάλυση CEA «η μέτρηση της αποτελεσματικότητας είναι σε
κερδισμένα έτη ζωής . Το μεγάλο πλεονέκτημα είναι ότι η ανθρώπινη ζωή και τα
υγειονομικά αποτελέσματα δεν αποτιμώνται
σε χρήμα, ενώ μόνο συστήματα, τεχνολογίες, προγράμματα ή υπηρεσίες με κοινές
μονάδες εκροών μπορούν να συγκριθούν1.
Στη
συγκεκριμένη μελέτη του Υ.Υ. επειδή «η οικονομική αξιολόγηση αφορά την επίτευξη
ή όχι του στόχου της μεγιστοποίησης των βελτιώσεων στην υγεία που παράγονται με ένα δεδομένο
επίπεδο δημόσιας δαπάνης , η κοινωνική δικαιοσύνη αφορά τη δίκαιη κατανομή των βελτιώσεων αυτών στο σύνολο του πληθυσμού6, ενδεδειγμένη είναι η ανάλυση του
κόστους αποτελεσματικότητας συγκριτικά ανάμεσα στις δύο
θεραπείες, καθόσον «η οικονομική αξιολόγηση κατευθύνει τη λήψη αποφάσεων
κατανομής πόρων μέσα στα πλαίσια καθορισμένων προϋπολογισμών, σε εκείνες τις
επιλογές που προσφέρουν τα μέγιστα δυνατά αποτελέσματα»1
«Στις
περισσότερες περιπτώσεις υπάρχουν διαφορές «στην ασφάλεια, αποτελεσματικότητα,
την τοξικότητα και την οικονομία των διάφορων εναλλακτικών θεραπευτικών επιλογών
για τους ασθενείς με καρκίνο»1
Το ίδιο συμβαίνει και δύο αυτές συγκριτικές αξιολογήσεις.
Τα αδύνατα
σημεία είναι ότι « ο προϋπολογισμός της θεραπευτικής παρέμβασης είναι
προσανατολισμένος στην πλευρά των εκροών και όχι των εισροών. Από την άλλη η
οριακή ανάλυση, προσπαθεί να εξετάσει το ενδεχόμενο μεταβολών στη χρήση των
πόρων μεταξύ προγραμμάτων υγείας με απώτερο σκοπό τη βελτίωση της κοινωνικής
ευημερίας. Αυτή συνίσταται στην εξέταση του αν μια μετατόπιση οικονομικών πόρων
κάποιου συγκεκριμένου ποσού από ένα πρόγραμμα υγείας σε κάποιο άλλο , επιφέρει
αύξηση του συνολικού οφέλους , δεδομένων των συνολικών διατιθέμενων πόρων.4
Βέβαια οι δύο δημόσιες θεραπείες
οφείλουν να δύνανται να κρίνουν και την αξία που προκύπτει εντός
της μακρόχρονης αποτελέσματος του
ατομικού συμφέροντος.1
«Επειδή
οι προϋπολογισμοί για την υγειονομική Περίθαλψη είναι περιορισμένοι, μπορεί να
καθοδηγήσει και να βοηθήσει τους υπεύθυνους για τη λήψη αποφάσεων να
μεγιστοποιήσουν την αξία των χρημάτων που δαπανώνται, δηλαδή τα χρόνια ζωής που
κερδίζονται ανά ευρώ».
Το ζήτημα
αυτό καθίσταται ακόμη πιο σημαντικό όταν κάποιος πρέπει να εξετάσει αν
προσθέσει ένα ακριβό παράγοντα – θεραπεία πάνω από έναν άλλο, για να βοηθήσει
τους ασθενείς να επιβιώσουν για ένα ή δύο ακόμη μήνες κατά μέσο όρο».5
Αυτό προκύπτει και στις 2 θεραπείες του καρκίνου του προστάτη. Το θέμα είναι
«αν αξίζει τα επιπλέον χρήματα».1
Έτσι με
γνώμονα την οικονομική δυσπραγία που υφίσταται στην χώρα μας , αλλά και των
δυνατοτήτων της ενόψει του μεσοπρόθεσμου , που μειώνουν αυξητικά τα έξοδα στο
χώρο της υγείας, καθίσταται αναγκαίο οι συγκριτικές αξιολογήσεις των
θεραπευτικών προσεγγίσεων να διαλέγουν εκείνες που θα αυξάνουν τα οφέλη για
τους αρρώστους με το χαμηλότερο εφικτό κόστος για τον χώρο της δημόσιας υγείας στην χώρα μας.1
«Καθόσον
στις περισσότερες χώρες γίνεται μια προσπάθεια , να γίνονται οικονομικές
αναλύσεις κόστους αποτελέσματος πριν υιοθετηθεί μια καινούργια ιατρική πρακτική,
οι πρωτοβουλίες κάποιων συστημάτων υγείας έχει εκφραστεί με την έκδοση
οικονομικών οδηγιών με τις κλινικές οδηγίες . Είναι 1 σημαντικό βήμα που θα
φέρει θετικές επιδράσεις στην οικονομική αποδοτικότητα. Οι οικονομικές οδηγίες
θα πρέπει να αναθεωρούνται συχνά ανάλογα με τις μεταβολές στους τομείς της
αγοράς, τις υγειονομικές ανάγκες, τα κλινικά δεδομένα και στην παραγωγικότητα.4
ΚΑΡΚΙΝΟΣ
ΠΡΟΣΤΑΤΗ
«O καρκίνος του προστάτη αποτελεί τη
συχνότερη νεοπλασματική νόσο στους άντρες με ετήσια επίπτωση 200/100.000
αντρών. Ο προληπτικός έλεγχος με τη μέτρηση του PSA που ξεκίνησε τα τελευταία
20 χρόνια οδήγησε στην πιο έγκαιρη διάγνωση της νόσου και στην αποτελεσματικότερη
θεραπεία της. Ο μαζικός πληθυσμιακός έλεγχος πιθανότατα είχε ως αποτέλεσμα και
την υπερδιάγνωση του καρκίνου του προστάτη, αφού παρατηρήθηκε σημαντική αύξηση
της επίπτωσης του και μόνο το 10‐15% αποβιώνει από αίτια που σχετίζονται με τη νόσο.
Α. ΑΣΘΕΝΕΙΣ ΜΕ ΒΙΟΧΗΜΙΚΗ ΥΠΟΤΡΟΠΗ ΜΕΤΑ ΑΠΟ ΤΟΠΙΚΗ
ΘΕΡΑΠΕΙΑ
Πρέπει να εκτιμώνται για την πιθανή
υποψηφιότητά τους για τοπική θεραπεία διασώσεως. O χρόνος έναρξης του
ανδρογονικού αποκλεισμού εξατομικεύεται ανάλογα με την ταχύτητα ανόδου PSA,
πιθανές επιπλοκές της θεραπείας, συνοσηρότητα και την σχετική αγωνία του ασθενούς
ως προς την παρακολούθηση της νόσου του. Ασθενείς με παρατεταμένο χρόνο διπλασιασμού
του PSA και μικρότερο προσδόκιμο επιβίωσης μπορούν να τεθούν σε πρόγραμμα
παρακολούθησης. Ασθενείς με βραχύ χρόνο διπλασιασμού του PSA και μεγάλο προσδόκιμο
επιβίωσης θα πρέπει να ενθαρρύνονται υπέρ της έγκαιρης έναρξης ανδρογονικού αποκλεισμού.
Οι ασθενείς που επιλέγουν θεραπεία ανδρογονικού αποκλεισμού μπορεί να επιλέξουν
διακοπτόμενο ανδρογονικό αποκλεισμό. Μία μελέτη φάσεως ΙΙΙ έδειξε ότι ο διακοπτόμενος
δεν ήταν κατώτερος από τον συνεχή ανδρογονικό αποκλεισμό. Μία αύξηση κατά 7%
στην θνητότητα από καρκίνο προστάτου στο σκέλος του διακοπτόμενου ανδρογονικού
αποκλεισμού αντιρροπίσθηκε από περισσότερους θανάτους μη σχετιζόμενους με
καρκίνο προστάτου στο σκέλος του συνεχούς ανδογονικού αποκλεισμού. Στην υποκατηγορία
των ασθενών με Gleasonscore 8‐10 (σε μή προγραμματισμένη σύγκριση)υπήρχε όφελος επιβίωσης στην ομάδα του
συνεχούς ανδρογονικού αποκλεισμού (διάμεση 8έτη έναντι 6,8 ετών).
Β. ΑΣΘΕΝΕΙΣ ΜΕ ΠΡΟΧΩΡΗΜΕΝΗ ΝΟΣΟ ΧΩΡΙΣ ΠΡΟΗΓΟΥΜΕΝΗ
ΕΚΘΕΣΗ ΣΕ ΑΝΔΡΟΓΟΝΙΚΟ ΑΠΟΚΛΕΙΣΜΟ
Μπορεί να αντιμετωπισθούν με τις κάτωθι επιλογές:
- Ορχιεκτομή,
- LHRH ανάλογα με ή χωρίς αντιανδρογόνο
τουλάχιστον για 7 ημέρες για την αποφυγήαπότομης επιδείνωσης (flare),
- LHRH ανταγωνιστές,
- Συνδυαστικό ανδρογονικό αποκλεισμό,
- Παρακολούθηση για ασυμπτωματικούς ασθενείς
χωρίς μεταστάσεις,
- Συνεχή ανδρογονικό αποκλεισμό μαζί με
χημειοθεραπεία με δοσεταξέλη (75mg/m2/3εβδομάδες) χωρίς πρεδνιζόνη για 6
κύκλους για ασθενείς με υψηλού φορτίου
μεταστατική
νόσο (πολλαπλές οστικές εντοπίσεις και σε εστίες εκτός σπονδυλικής στήλης
/πυέλου ή / και σπλαχνικές μεταστάσεις). Η χημειοθεραπεία δεν πρέπει να
χορηγείται σε ασθενείς με ορμονο‐ευαίσθητο καρκίνο προστάτη χωρίς μεταστάσεις ή σε ασθενείς με χαμηλού
φορτίου μεταστατική νόσο .
- Διακοπτόμενο ανδρογονικό αποκλεισμό σε
μετασταστικούς ασυμπτωματικούς ασθενείς που παρουσιάζουν πολλές επιπλοκές
από τον συνεχή ανδρογονικό αποκλεισμό, αναγνωρίζοντας ότι ο διακοπτόμενος
ανδρογονικός αποκλεισμός επιβάλλει στενή παρακολούθηση του PSA και
τεστοστερόνης ορού, ειδικά στα μεσοδιαστήματα χωρίς θεραπεία, και ότι οι
ασθενείς θα χρειαστεί να επιστρέψουν σε συνεχή ανδρογονικό αποκλεισμό όταν
υπάρξουν ενδείξεις επιδείνωσης της νόσου.
Γ. ΟΣΤΙΚΗ ΥΓΕΙΑ ΚΑΤΑ ΤΗΝ ΔΙΑΡΚΕΙΑ ΑΝΔΡΟΓΟΝΙΚΟΥ
ΑΠΟΚΛΕΙΣΜΟΥ
Χρειάζεται έλεγχος και θεραπεία οστεοπορώσεως
σύμφωνα με τις διεθνείς οδηγίες:
1.
Συμπλήρωμα ασβεστίου (1200 mg/ημέρα) και βιταμίνη
D3 (800‐1000 IU/ημέρα)
για όλουςτους άνδρες > 50 ετών.
2.
Πρόσθετη θεραπεία για άνδρες με > 3% 10‐ετή κίνδυνο για κάταγμα ισχίου ή για άνδρες
με> 20% κίνδυνο για οστεοπορωτικό κάταγμα, σύμφωνα με τον αλγόριθμο FRAX® της
Π.Ο.Υ.που είναι α) denosumab 60 mgsq/ 6μήνες, ή β) zolendronicacid 5 mgiv / έτος,
ή γ) alendronate70 mgpo / εβδομάδα.
Δ. ΕΥΝΟΥΧΟΑΝΤΟΧΟΣ ΚΑΡΚΙΝΟΣ ΠΡΟΣΤΑΤΗ
Ο καρκίνος του προστάτη χαρακτηρίζεται ως
ευνουχοάντοχος, μόνο όταν υπάρχει βιοχημική ένδειξη πως είχε επιτευχθεί ο
ανδρογονικός αποκλεισμός (επίπεδα τεστοστερόνης ορού < 50ng/dl) και υπάρχει
κλινική ή και βιοχημική επιδείνωση νόσου μετά και την απόσυρση αντι‐ανδρογόνου αν είχε χρησιμοποιηθεί.
Δ1. ΕΥΝΟΥΧΟΑΝΤΟΧΟΣ ΜΗ‐ΜΕΤΑΣΤΑΤΙΚΟΣ
ΚΑΡΚΙΝΟΣ ΠΡΟΣΤΑΤΗ
Όλοι οι ασθενείς πρέπει να διατηρούν επίπεδα
ευνουχισμού τεστοστερόνης ορού
- Κλινική μελέτη
- Παρακολούθηση, ειδικά αν ο χρόνος διπλασιασμού
του PSA ορού είναι > από 10 μήνες
- Δεύτερης γραμμής ορμονικοί χειρισμοί, ειδικά
αν ο χρόνος διπλασιασμού του PSA ορού είναι < από 10 μήνες
a.
Αντιανδρογόνο
b.
Απόσυρση αντιανδρογόνου (αν το ελάμβανε ο ασθενής)
c.
Κετοκοναζόλη (με υποκατάσταση υδροκορτιζόνης)
d.
Χαμηλές δόσεις στεροειδών (π.χ. Prednisone 5 mg /
ημέρα)
e.
Χαμηλές δόσεις οιστρογόνων σε ασθενείς χωρίς
καρδιαγγειακά προβλήματα(π.χ. DES 1‐2 mg /day).
Δ2. ΜΕΤΑΣΤΑΤΙΚΟΣ ΕΥΝΟΥΧΟΑΝΤΟΧΟΣ ΚΑΡΚΙΝΟΣ
ΠΡΟΣΤΑΤΟΥ
Όλοι οι
ασθενείς πρέπει να διατηρούν επίπεδα ευνουχισμού τεστοστερόνης ορού και να
δέχονται την βέλτιστη υποστηρικτική
θεραπεία.
Δ2α. ΤΡΙΤΕΥΟΝΤΕΣ ΟΡΜΟΝΙΚΟΙ ΧΕΙΡΙΣΜΟΙ
Για
ασυμπτωπατικούς μεταστατικούς ασθενείς χωρίς σπλαχνικές μεταστάσεις προ
χημειοθεραπείας με δοσεταξέλη ή ασυμπτωπατικούς /ήπια συμπτωματικούς μεταστατικούς
ασθενείς μετά από χημειοθεραπεία με δοσεταξέλη:
- Abirateroneacetate, 1000mg/ημέρα πρό φαγητού
σε συνδυασμό με πρεδνιζόνη 5mg δύο φορές την ημέρα, ως θεραπεία 2ης
γραμμής (κατηγορία 1).
- Enzalutamide 160 mg /ημέρα, με ή χωρίς φαγητό
– με ή χωρίς πρεδνιζόνη (προσοχή σε συγχορηγούμενα φάρμακα – ειδικά
πραζόλες), ως θεραπεία 2ης γραμμής (κατηγορία 1).
Δ2β. ΧΗΜΕΙΟΘΕΡΑΠΕΙΑ ΜΕΤΑΣΤΑΤΙΚΟΥ
ΕΥΝΟΥΧΟΑΝΤΟΧΟΥ ΚΑΡΚΙΝΟΥ ΠΡΟΣΤΑΤΗ
1.
Docetaxel 75 mg/m², IV + Prednisolone 5mg δις/ημέρα
(για όλη τη διάρκεια του κύκλου), PO κάθε 21 μέρες
2.
Docetaxel 60‐70 mg/m² (ημέρα 2), IV + Estramustine280 mg (2 tablets) 3 φορές / ημέρα(ημέρες
1‐5), PO,
Dexamethasone 20 mgPO κάθε 12 ώρες χ 3 φορές (ημέρες 1‐2 ) κάθε 21ημέρες
3.
Mitoxantrone 12mg/m², IV + Prednisolone 5mg
δις/ημέρα,PO, κάθε 21 μέρες
4.
Vinorelbine 25‐30mg/m² IVή 60‐80 mg/m², ημέρες
1, 8, PO + Prednisolone 5mg δις/ημέρα,PO, κάθε 21 μέρες
5.
Cabazitaxel, 25mg/m2, IV + Prednisone ή
Prednisolone 10mg/ημέρα (καθ’ όλη τη διάρκεια της θεραπείας), ως θεραπεία 2ης
γραμμής μετά από θεραπευτικό σχήμα που περιείχε docetaxel, με προφύλαξη με
GCSF, κάθε 21 ημέρες
6.
Ένταξη σε κλινική μελέτη.
Δ2γ. ΟΣΤΙΚΗ ΣΤΟΧΕΥΣΗ ΜΕΤΑΣΤΑΤΙΚΟΥ
ΕΥΝΟΥΧΟΑΝΤΟΧΟΥ ΚΑΡΚΙΝΟΥ ΠΡΟΣΤΑΤΗ
1.
Σε ασθενείς με οστικές μεταστάσεις συστήνεται ένα
από τα ακόλουθα για πρόληψη σκελετικών συμβαμάτων (παθολογικά κατάγματα,
συμπίεση νωτιαίου μυελού,, ανάγκη χειρουργικής παρέμβασης ή ακτινοθεραπείας)
(κατηγορία 1) με συγχορήγηση ασβεστίου και βιταμίνης D, αν και η βέλτιστη
διάρκεια θεραπείας με αυτούς τους παράγοντες δεν είναι γνωστή:
Ι. Ζολεδρονικό οξύ (4 mg/3‐4 εβδομάδες iv) με παρακολούθηση νεφρικής λειτουργίας,ή
ΙΙ. Μονοκλωνικό anti‐RANKL αντίσωμα Denosumab (120mg/4 εβδομάδες
sq)
2.
Το Radium‐223 (Xofigo / Alpharadin) (α‐emitter) είναι εγκεκριμένο για θεραπεία συμπτωματικών οστικών
μεταστάσεων ευνουχο‐άντοχου καρκίνου
προστάτη απουσία σπλαχνικών μεταστάσεων με βελτίωση συμπτωμάτων και συνολικής
επιβίωσης (κατηγορία1). Μπορεί να συγχορηγηθεί με denosumab ή διφωσφονικά, ενώ
η συγχορήγησή του με χημειοθεραπεία αυξάνει την αιματολογική τοξικότητα.
3.
Συστηματική ακτινοθεραπεία είτε με 89Sr είτε με
153Sm μπορεί να έχει παρηγορική δράση σε ορισμένους συμπτωματικούς ασθενείς με
εκτεταμένες οστικές μεταστάσεις που δεν απαντούν ή δεν είναι υποψήφιοι για
χημειοθεραπεία ή εξωτερική ακτινοθεραπεία και δεν απαντούν σε συστηματική
αναλγητική αγωγή, αλλά συνδυάζονται με βραχεία ανταπόκριση και μεγαλύτερη
μυελοτοξικότητα (β‐emitters) σχέση
το Radium‐223 (Xofigo
/ Alpharadin).
Σημείωση
1: Η χημειοθεραπεία να δίδεται μόνο σε ασθενείς
με μεταστατικό ευνουχοάντοχο καρκίνο προστάτη. Υπ’ αυτήν την έννοια
ορμονοθεραπείες 2ης γραμμής, αλλαγή απόσυρση αντι-ανδρογόνων, κετοκοναζόλη,
κορτικοστεροειδή, καλό είναι να χορηγούνται στους ασθενείς πριν από την έναρξη
της χημειοθεραπείας. Εξαίρεση αποτελούν οι ασθενείς με μεταστατικόορμονο εξαρτώμενο
καρκίνο προστάτη και υψηλό φορτίο μεταστατικής νόσου (ίδε Β6ανωτέρω).
Σημείωση
2: Τα GnRH ανάλογα θα πρέπει να συνεχίζονται μαζί
με τη χημειοθεραπεία (τα
Επίπεδα τεστοστερόνης
να είναι <50 ng/dl). Η χορήγηση αντι-ανδρογόνων θα πρέπει να έχει διακοπεί τουλάχιστον
4 εβδομάδες πριν από την έναρξη της χημειοθεραπείας εκτός από τα περιστατικά μεταστατικού
μικροκυτταρικού καρκίνου προστάτη όπου δεν
αναμένεται απάντηση στην απόσυρση αντι‐ανδρογόνου και η χημειοθεραπεία πρέπει να μην καθυστερεί.
Σημείωση
3: H υποψία ύπαρξης μικροκυτταρικού καρκίνου προστάτη
τίθεται σε ασθενείς με υψηλό αρχικό Gleasonscore (9‐10), χαμηλό PSA ορού για
το φορτίο νόσου και συνήθως απουσία ή βραχεία απάντηση στην αρχική ορμονική θεραπεία.
Σε αυτούς τους ασθενείς ενδείκνυται επανάληψη βιοψίας προσβάσιμης εστίας για ιστολογική
ταυτοποίηση. Αυτοί οι ασθενείς μπορούν να αντιμετωπισθούν με χημειοθεραπευτικά σχήματα
όπως σισπλατίνη/ετοποσίδη, καρβοπλατίνη/ετοποσίδη ή σχήματα βασισμένα σε δοσεταξέλη
ή ένταξησε κλινική μελέτη. Ο ιασθενείς με νευροενδοκρινή διαφοροποίηση διαφέρουν
από τους ασθενείς με μικροκυτταρικό καρκίνο προστάτη. Νευροενδοκρινή διαφοροποίηση
είναι πολύ πιο συχνή και προς το παρόν δεν υπάρχουν στοιχεία που να υπαγορεύουν
αλλαγή θεραπευτικής αντιμετώπισης.
Σημείωση
4: Σε ασθενείς με μεταστατικό ευνουχοάντοχο καρκίνο
προστάτου μετά από
Χημειοθεραπεία
με δοσεταξέλη και η οξεική αμπιρατερόνη (μεπρεδνιζόνη) και η ενζαλουταμίδη έδειξαν
όφελος συνολικής επιβίωσης (κατηγορία I). Δεν υπάρχει προς το παρόν ένδειξη βάσει
μελετών για την βέλτιστη αλληλουχία αυτών των θεραπειών μετά από χημειοθεραπεία.
Σημείωση
5: Και στις δύο μελέτες (αμπιρατερόνης και ενζαλουταμίδης)
σε ασθενείς με
Μεταστατικό
ευνουχοάντοχο καρκίνο προστάτου προχημειοθεραπείας με δοσεταξέλη.
Εισήχθησαν
ασθενείς είτε χωρίς είτε με λίγα συμπτώματα από την μεταστατική τους νόσο. Σε ασθενείς
με σημαντικά συμπτώματα (π.χ. έντονα οστικά άλγη) δεν υπάρχει προς το παρόν σύγκριση
για την παρηγορική τους δράση σε σχέση με χημειοθεραπεία με δοσεταξέλη. Η οξεική
αμπιρατερόνη και ηνζαλουταμίδη είναι εγκεκριμένες για χορήγηση σε ασθενείς με μεταστατικό
ευνουχοάντοχο καρκίνο προστάτου χωρίς ή με λίγα συμπτώματα προ χημειοθεραπείας με
δοσεταξέλη (κατηγορία Ι).
Σημείωση
6: Συστήνεται έλεγχος και ιατρική παρέμβαση για
πρόληψη / θεραπεία σακχαρώδους διαβήτου και καρδιαγγειακής νόσου σε ασθενείς υπό
ανδρογονικό αποκλεισμό.
ΦΑΡΜΑΚΑ‐ΕΓΚΡΙΣΕΙΣ
Όλα τα προαναφερθέντα φάρμακα έχουν πάρει επίσημη
έγκριση για τη νόσο:
- Docetaxel
- Estramustin
- Mitoxantrone
- Vinorelbine
- Cabazitaxel
- Αbiraterone (Zytiga)
- Denosumab (XGEVA/ Prolia)
- Zolendronic acid (Zometa)
- Alendronate (Fosamax)
- 10.Enzalutamide (Xtandi)
- 11.Radium‐223 (Xofigo, previously Alpharadin)
- 12.Strontium‐89 (Metastron)
- 13.153‐Samarium (Lexidronam)»51
Το κόστος
φαρμάκων στη διαχείριση του μεταστατικού ανθεκτικού στον ευνουχισμό καρκίνου
του προστάτη στον Καναδά
«Μέθοδοι: Χρησιμοποιήθηκαν
δύο μοντέλα Markov με μικρο-προσομοιώσεις Monte-Carlo προκειμένου να
προσομοιωθεί η διαχείριση της νόσου και να εκτιμηθεί το κόστος θεραπείας
φαρμάκων στο mCRPC, σύμφωνα με το σύστημα δημόσιας υγειονομικής περίθαλψης του
Κεμπέκ. Τα μοντέλα περιλαμβάνουν πρόσφατα εγκεκριμένες πρόσθετες γραμμές
θεραπείας μετά ή πριν από τη δοκεταξέλη (δηλαδή abiraterone και cabazitaxel). Η
έκθεση σε φάρμακα και η επιβίωση βασίστηκαν σε αποτελέσματα κλινικών δοκιμών
και κατευθυντήριες γραμμές κλινικής πρακτικής που βρέθηκαν σε ανασκόπηση της
βιβλιογραφίας. Όλες οι δαπάνες καταλογίστηκαν σε δολάρια Καναδά ($) του 2013 [στην
παρούσα εργασία έχουμε μετατρέψει όλα τα νούμερα που αναφέρονται σε καναδικά
δολάρια σε αμερικάνικα δολάρια και στο κείμενο και στους πίνακες].Υπολογίστηκαν
μόνο τα άμεσα κόστη φαρμάκων.
Αποτελέσματα: Το μέσο
κόστος για τις φαρμακευτικές θεραπείες του mCRPC κατά την διάρκεια μιας μέσης
περιόδου 28,1 μηνών υπολογίστηκε σε 37,774 δολάρια ανά ασθενή (95% διάστημα
εμπιστοσύνης: 37,147 έως 38,401 δολάρια). Το μέσο κόστος αυξήθηκε σε 81,156
δολάρια (95% CI: 79,832 – 82,480 δολάρια) ανά ασθενή, όταν κάποιος
συμπεριλάμβανε την έναρξη της αμπιρατερόνης (=abiraterone) πριν από τη θεραπεία με docetaxel
(=δοκεταξέλη). Κατά τη διάρκεια της περιόδου mCRPC, οι αγωνιστές απελευθέρωσης
ορμόνης λουτεϊνοποίησης/ωχρινοτρόπου (LHRHa) που συνταγογραφήθηκαν για τη
διατήρηση των επιπέδων τεστοστερόνης ευνουχισμού αντιπροσώπευαν το 20,4% του
συνολικού κόστους φαρμακευτικής αγωγής, ενώ το denosumab που συνταγογραφήθηκε
για τη μείωση των σχετικών με οστικές εκδηλώσεις αντιπροσώπευε το 30,5% του
κόστους. Όταν οι ασθενείς έλαβαν καμπαζιταξέλη (=cabazitaxel) στη σειρά μετά από την αμπιτατερόνη και
δοκεταξέλη, τα κόστη για τα φάρμακα για mCRPC ανά ασθενή ανά μήνα αυξήθηκαν
κατά 60,2%. Το συνολικό κόστος των φαρμάκων για τη θεραπεία κάθε ετήσιας
καναδικής ομάδας 4.000 ασθενών με mCRPC εκτιμήθηκε από 151 εκατομμύρια έως 324
εκατομμύρια δολάρια.
Συμπεράσματα: Η μελέτη μας
εκτιμά το άμεσο κόστος των φαρμάκων που σχετίζονται με τις θεραπείες mCRPC στο
καναδικό σύστημα υγειονομικής περίθαλψης. Οι πρόσφατα προσδιορισμένες
αποτελεσματικές αλλά μη εγκεκριμένες θεραπείες θα γίνουν μέρος του φάσματος των
θεραπειών mCRPC και ενδέχεται να αυξήσουν το κόστος.
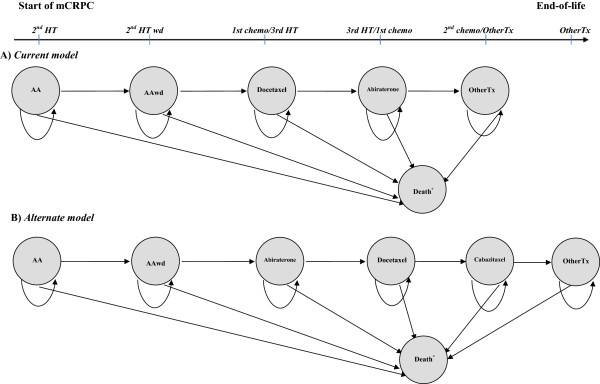
Εικόνα 1
Κύρια
ακολουθία θεραπείας σε περίοδο mCRPC: Α) Τρέχον μοντέλο. Β) Εναλλακτικό
μοντέλο. Οι οβάλ / κύκλοι υποδηλώνουν καταστάσεις σχετικές με τη θεραπεία.
Ευθεία βέλη που συνδέουν δύο διαφορετικές καταστάσεις που σχετίζονται με τη
θεραπεία δείχνουν ότι ο ασθενής μπορεί να κινηθεί σε μια επακόλουθη κατάσταση
θεραπείας κατά τη διάρκεια κάθε μηνιαίου κύκλου. Τα σύντομα καμπύλα βέλη που
οδηγούν από την κατάσταση της θεραπείας στο ίδιο δείχνουν ότι ο ασθενής μπορεί
να παραμείνει σε αυτή την κατάσταση σε διαδοχικούς κύκλους. Συντομογραφίες:
mCRPC = έναρξη της κατάστασης mCRPC, 2η HT = ορμονοθεραπεία δεύτερης γραμμής,
2η HT wd = δεύτερη γραμμή απόσυρση ορμονοθεραπείας. 1η χημειοθεραπεία =
χημειοθεραπεία πρώτης γραμμής. 3η HT = ορμονοθεραπεία τρίτης γραμμής, 2η
χημειοθεραπεία = χημειοθεραπεία δεύτερης γραμμής. OtherTx = κατάσταση άλλες θεραπείες
ΑΑ = κατάσταση αντιανδρογόνων AAwd = κατάσταση απόσυρσης αντιανδρογόνων, * Η
κατάσταση του θανάτου ενσωματώνει τόσο τον καρκίνο του προστάτη όσο και τις μη
σχετικές αιτίες θανάτου.
Αναλύσεις
κόστους: Το κόστος των φαρμακευτικών θεραπειών στη φάση mCRPC εκτιμήθηκε συνολικά
(συνολικό κόστος), με συγκεκριμένες γραμμές θεραπείας και ταξινομήθηκε σε: 1)
το κόστος πρωτογενούς φαρμακευτικής αγωγής (απόκτηση φαρμάκου, κόστος χορήγησης
και φάρμακα προθεραπείας που χρησιμοποιήθηκαν ως προφυλακτικά φάρμακα για
προκαλούμενες από χημειοθεραπεία παρενέργειες, π.χ. δεξαμεθαζόνη (=dexamethasone )· 2) το
κόστος του ιατρικού ευνουχισμού για τη διατήρηση των επιπέδων τεστοστερόνης
(LHRHa)· και 3) το κόστος των θεραπειών με στόχο τα οστά, οι οποίες
αποτελούνται από φάρμακα που χρησιμοποιούνται για την πρόληψη των σχετιζόμενων
με το σκελετικό συμβάντων (denosumab = δενοσουμάμπη ή zoledronicacid = ζολεδρονικό
οξύ). Κατά τη διάρκεια της περιόδου mCRPC, το 95% και το 90% των ασθενών
υποτίθεται ότι έλαβαν τον ιατρικό ευνουχισμό και τη θεραπεία με στόχο τα οστά,
αντίστοιχα. Το συνολικό κόστος καρκίνου του mCRPC από τον Καναδά εκτιμήθηκε
πολλαπλασιάζοντας τον αριθμό των ασθενών που ταξίδεψαν στην/πέρασαν από την
περίοδο mCRPC πριν από το τέλος της ζωής τους (θεωρούμενος ότι είναι ίσος με
τον αριθμό των θανάτων PCa το 2012 στον Καναδά), με το μέσο κόστος φαρμάκων
κατά την περίοδο mCRPC.
Ανάλυση ευαισθησίας:
Δεδομένου
ότι δεν υπάρχουν διαθέσιμα στοιχεία στη βιβλιογραφία που να περιγράφουν τα
ποσοστά χρήσης φαρμακευτικής αγωγής σε mCRPC (δηλ. το ποσοστό των ασθενών που
προχωρούν από τη μια γραμμή θεραπείας στην άλλη), δοκιμάστηκαν διάφορα σενάρια
μεταβάλλοντας (αυξάνοντας ή / και μειώνοντας) το ποσοστό των ασθενών που έλαβαν
τις πιο δαπανηρές θεραπείες. Αυτά τα σενάρια πιθανολογούνται ότι έχουν τον
σημαντικότερο αντίκτυπο στις εκτιμήσεις κόστους. Επιπλέον, ο σημερινός
πληθυσμός που λαμβάνει ειδική θεραπεία μπορεί να διαφέρει από τον πληθυσμό σε
κλινικές δοκιμές. Ως εκ τούτου, σύμφωνα με τη γνώμη των εμπειρογνωμόνων, τα
ακόλουθα τέσσερα σενάρια θεωρήθηκαν εύλογα στην πραγματική κλινική πρακτική και
έχουν ελεγχθεί. Το πρώτο σενάριο
θεώρησε μια διακύμανση 10% και 20% της πιθανότητας μετάβασης από το docetaxel
σε επακόλουθη θεραπεία. Τοσενάριο 2)
υπέθεσε ότι το 20%, 30% και το 50% των ασθενών έλαβαν επαναθεραπεία με
docetaxel μετά από το docetaxel . Το σενάριο 3) υπέθεσε ότι το 50%, το 70% και το 100% των ασθενών έλαβαν μέγιστο
αποκλεισμό ανδρογόνων πριν εισέλθουν στη φάση mCRPC, έτσι ώστε η φάση mCRPC
ξεκινά με την έναρξη του docetaxel (τρέχον μοντέλο ) και του abiraterone
(εναλλακτικό μοντέλο). Τέλος, το σενάριο
4) υποθέτει ότι το 90%, το 80% και το 70% των ασθενών έλαβαν απευθείας
δοκεταξέλη (τρέχον μοντέλο) ή abiraterone (εναλλακτικό μοντέλο)μετά από ΑΑ
(αντιανδρογόνο).
Πιθανότητες
και εκτιμήσεις κόστους: Η μηνιαία πιθανότητα θανάτου, η πιθανότητα μετάβασης
στην επόμενη γραμμή θεραπείας και η πιθανότητα διαμονής στην ίδια γραμμή
θεραπείας υπολογίστηκαν για κάθε γραμμή θεραπείας (τα δεδομένα δεν
παρουσιάζονται). Οι μονάδες και το μηνιαίο κόστος των φαρμάκων παρατίθενται
στον Πίνακα 2. Το πρωτογενές κόστος φαρμακευτικής αγωγής κυμάνθηκε από 46
δολάρια ανά ασθενή το μήνα για τη βικαλουταμίδη (bicalutamide), στα 6596 δολάρια ανά ασθενή το μήνα για
το cabazitaxel. Οι αντίστοιχες τιμές για τον ιατρικό ευνουχισμό και τη θεραπεία
με στόχο τα οστά υπολογίζονται σε 289 δολάρια (κόστος οξικής γοσερελίνης (goserelinacetate)) και 455
δολάρια (κόστος denosumab / zoledronicacid), αντίστοιχα
Πίνακας 12:Μονάδα και
μηνιαίο κόστος των φαρμάκων mCRPC
Φαρμακευτική αγωγή
Δοσολογία (αναφορά) Κόστος ανά
μονάδα (αναφορά) Κόστος ανά
μήνα
Πρωτογενής φαρμακευτική αγωγή
|
Bicalutamide
(Casodex) |
1
× 50 mg καθημερινά |
[17] |
$1.25
ανά δισκίο (50 mg) |
[42] |
$45.78 |
|
|
|
Abiraterone
(Zytiga) |
4
× 250 mg καθημερινά |
[34] |
$22.0914
ανά δισκίο (250 mg) |
[42] |
$2,688 |
|
|
|
Cabazitaxel
(Jevtana) |
25 mg/m2i.v. κάθε 21 μέρες |
[36] |
$4,553
ανά φιαλίδιο (60 mg/1.5 ml) |
[46] |
$6,596* |
|
|
|
Docetaxel
(Taxotere) |
75 mg/m2i.v.
κάθε 21 μέρες |
[26] |
$467.68ανάφιαλίδιο (160 mg/16 ml)** |
[46] |
$603* |
|
|
|
Prednisone (Deltasone) |
2
× 5 mg καθημερινά |
[34] |
$0.017
ανά δισκίο (5 mg)** |
[42] $1.02 |
|||
|
Προθεραπευτική
αγωγή για παρενέργειες που προκαλούνται από την χημειοθεραπεία |
|
||||||
|
Dexamethasone†‡ |
8 mgi.v. κάθε 21 μέρες |
|
$2.52ανά
φιαλίδιο (10 mg/ml, 1 ml)** |
[46] |
$3.65 |
|
|
|
Diphenhydramine† |
25 mg i.v.κάθε 21 μέρες |
[36] |
$2.32
ανά φιαλίδιο (50 mg/ml, 1 ml)** |
[46] |
$3.36 |
|
|
|
Famotidine† |
20 mg i.v.κάθε 21 μέρες |
[36] |
$2.11
ανά φιαλίδιο (10 mg/ml, 2 ml)** |
[46] |
$3.06 |
|
|
|
Φάρμακα για
ιατρικό ευνουχισμό |
|
||||||
|
Goserelin
(Zoladex) |
10.8 mg s.c. κάθε 3 μήνες (13 βδομάδες) |
[40] |
$867
ανά 10.8 mg ένεση αποθήκης (depot) 3
μηνών |
[42] |
$289 |
|
|
|
Θεραπεία
με στόχο τα οστά |
|
||||||
|
Denosumab
(XGEVA) |
120 mg s.c. κάθε 4 βδομάδες |
[23] |
$419.52ανά φιαλίδιο (120 mg/1.7 ml) |
[42] |
$455 |
|
|
*Βάσει
της επιφάνειας σώματος 1,9 m2. Αυτό αντιστοιχεί στις κανονικές τιμές
που αναφέρθηκαν για τους άνδρες στο γενικό πληθυσμό [47]. Το μηνιαίο κόστος
χημειοθεραπείας υπολογίστηκε με την παραδοχή ότι οι ασθενείς δεν μοιράζονται τα
φιαλίδια.
** Κόστος γενικής χρήσης.
† Προ-φαρμακευτική αγωγή για cabazitaxel.
‡ Προ-φαρμακευτική αγωγή για docetaxel .
Πηγή: Alice Dragomir, Daniela Dinea, [...], and
Armen G Aprikian
Η προσομοίωση της ακολουθίας θεραπείας, η
διάρκεια των θεραπειών, η επιβίωση σε mCRPC και η εγκυρότητα των προγνωστικών
μοντέλων
Ο Πίνακας 3 παρουσιάζει το ποσοστό των ασθενών που έλαβαν κάθε γραμμή
θεραπείας, τη διάρκεια κάθε συγκεκριμένης κατάστασης θεραπείας και την
επιβίωση, όπως προσομοιώνεται από τα μοντέλα Current(Τρέχον) και Alternative
(Εναλλακτικό). Και τα δύο μοντέλα υποθέτουν ότι η φάση mCRPC ξεκινά με
αποκλεισμό αντιανδρογόνων. Επομένως, όλοι οι προσομοιωμένοι ασθενείς ξεκινούν από
την κατάσταση ΑΑ. Το Τρέχον μοντέλο προσομοιώνει ότι από όλους τους ασθενείς
που ξεκινούν με ΑΑ, το 88,1% πέρασε στο AAwd, το 72,5% έλαβε docetaxel και το
54,2% έλαβε abiraterone. Με το Εναλλακτικό μοντέλο οι αντίστοιχες τιμές ήταν:
AAwd (88,0%), abiraterone (72,6%), docetaxel (47,4%) και cabazitaxel (34,4%).
Κατά την παρακολούθηση, το 29,4% και το 26,9% των ασθενών, στα μοντέλα Current
και Alternate αντίστοιχα, ήταν ακόμα ζωντανοί στο τέλος των ακολουθιών
θεραπείας και μεταφέρθηκαν στο OtherTx. Επιπλέον, η διάμεση διάρκεια θεραπείας
στο μοντέλο Current κυμαίνονταν από 4 μήνες (IQR: 3-6) για AAwd έως 9 μήνες
(IQR: 4-17) για abiraterone, ενώ κυμαινόταν από 4 μήνες (IQR: 3-6) για AAwd έως
19 μήνες (IQR: 9-35) για abiraterone στο εναλλακτικό μοντέλο. Η διάμεση
συνολική επιβίωση σε mCRPC υπολογίστηκε σε 25 μήνες (IQR: 14-40) στο μοντέλο
Current και 34 μήνες (IQR: 15-56) στο εναλλακτικό μοντέλο, αντίστοιχα.
Πίνακας
13:Προσομοιωμένες αλληλουχίες θεραπείας, διάρκεια των
θεραπειών ανά ασθενή, και η επιβίωση σε mCRPC
|
Τρέχον Μοντέλο (Current) |
|
|
|
|
|
|
|
Αλληλουχία θεραπείας |
AA |
AAwd |
Docetaxel |
Abiraterone |
OtherTx |
|
|
% των ασθενών που υποβάλλονται σε κάθε γραμμή θεραπείας |
100% |
88.1% |
72.7% |
54.2% |
29.4% |
|
|
Μέση διάρκεια ανά ασθενή (95%CI)* |
8.5 (8.4-8.6) |
4.3 (4.3-4.4) |
7.1 (7.0-7.1) |
10 (9.9-10.2) |
14.6 (14.3-14.9) |
|
|
Διάμεση (median) διάρκεια ανά ασθενή (IQR)* |
8 (5–12) |
4 (3–6) |
7 (7–8) |
9 (4–17) |
15 (6–24) |
|
|
Μέση Επιβίωση (95%CI)** |
28.1 (27.7-28.4) |
22.1 (21.7-22.4) |
21.3 (20.9-21.6) |
18.8 (18.4-19.1) |
15.2 (14.9-15.5) |
|
|
Διάμεση (Median) Επιβίωση (IQR)** |
25 (14–40) |
19 (7–24) |
18 (9–32) |
16 (8–28) |
16 (7–24) |
|
|
Εναλλακτικό μοντέλο (Alternate) |
|
|
|
|
|
|
|
Αλληλουχία
θεραπείας |
AA |
AAwd |
Abiraterone |
Docetaxel |
Cabazitaxel |
OtherTx |
|
% των ασθενών που υποβάλλονται σε κάθε γραμμή θεραπείας |
100% |
88.0% |
72.6% |
47.4% |
35.4% |
26.9% |
|
Μέση διάρκεια ανά ασθενή (95%CI)* |
8.6 (8.5-8.7) |
4.4 (4.3-4.4) |
20.2 (19.9- 20.4) |
7.0 (7.0-7.1) |
5.7 (5.6-5.8) |
15.0 (14.7-15.4) |
|
Διάμεση διάρκεια ανά ασθενή (IQR)* |
8 (5–12) |
4 (3–6) |
19 (9–35) |
7 (7–8) |
5 (4–7) |
16 (7–24) |
|
Μέση Επιβίωση (95%CI)** |
37.3 (36.8-37.8) |
32.5 (32.0-32.9) |
33.8 (33.4.0-34.3) |
20.4 (20.1-20.8) |
17.6 (17.3-17.9) |
15.7 (15.4-16.0) |
|
Διάμεση Επιβίωση (IQR)** |
34 (15–56) |
30.0 (12–50) |
32 (17–48) |
18 (9–34) |
17 (8–28) |
17 (8–24) |
*σε κάθε κατάσταση συγκεκριμένης
θεραπείας (95% CI) (μήνες). ** από την είσοδο στην ειδική κατάσταση της
θεραπείας (IQR: 25 και 75 εκατοστημόρια).
Συντομογραφίες: 95% CI 95% διάστημα
εμπιστοσύνης, IQR Διατεταρτημοριακό
εύρος , ΑΑ αντιανδρογόνο, AAwd Απόσυρση αντιανδρογόνου, OtherTx Άλλες
θεραπείες.
Πηγή: Alice Dragomir, Daniela Dinea, [...], and
Armen G Aprikian
Εκτιμώμενο
κόστος των φαρμάκων mCRPC ανά γραμμή θεραπείας
Ο
Πίνακας 14 παρουσιάζει το μέσο κόστος κάθε γραμμής θεραπείας σε ασθενείς που
λαμβάνουν αυτή τη γραμμή θεραπείας, το σύνολο και ανά τύπο φαρμάκου.
Πίνακας 14: Κόστος
πρωτογενούς φαρμακευτικής αγωγής, φαρμάκων για ιατρικό ευνουχισμό, θεραπείας με
στόχο τα οστά ανά ασθενή, κατά γραμμή θεραπείας για mCRPC
|
Ακολουθία θεραπείας |
Πρωτογενής φαρμακευτική αγωγή |
Φάρμακα για ιατρικό ευνουχισμό * |
Θεραπεία με στόχο τα οστά ** |
Σύνολο |
||||
|
Τρέχον μοντέλο |
Μέσο κόστος (95%CI) |
Διάμεσο κόστος (IQR) |
Μέσο κόστος (95%CI) |
Διάμεσο κόστος (IQR) |
Μέσο κόστος (95%CI) |
Διάμεσο κόστος (IQR) |
Μέσο κόστος (95%CI) |
Διάμεσο κόστος (IQR) |
|
AA |
$390 |
$320 |
$2,342 |
$1,924 |
$3,498 |
$2,875 |
$6,230 |
$5,119 |
|
($386-$394) |
($228-$550) |
($2,318-$2,365) |
($1,374-$3,298) |
($3,463-$3,533) |
($2,053-$3,928) |
($6,167-$6,292) |
($3,656-$8,775) |
|
|
AAwd |
$0 |
$0 |
$1,190 |
$1,099 |
$1,778 |
$1,642 |
$2,968 |
$2,741 |
|
|
|
($1,180-$1,199) |
($0,824-$1,650) |
($1,765-$1,793) |
($1,232-$2,464) |
($2,944-$2,992) |
($2,056-$4,120) |
|
|
Docetaxel |
$4,814 |
$4,776 |
$1,939 |
$1,924 |
$2,897 |
$2,875 |
$9,651 |
$9,576 |
|
($4,778-$4,851) |
($4,777-$5,459) |
($1,924-$1,955) |
($1,924-$2,199) |
($2,876-$2,920) |
($2,875-$3,285) |
($9,578-$10,505) |
($9,576-$10,944) |
|
|
Abiraterone |
$27,007 |
$24,211 |
$2,760 |
$2,474 |
$4,122 |
$3,696 |
$33,889 |
$30,381 |
|
($26,545-$27,469) |
($10,761-$45,732) |
($2,712-$2,807) |
($1,099-$4,673) |
($4,052-$4,193) |
($1,643-$6,981) |
($33,311-$34,470) |
($13,503-$57,387) |
|
|
OtherTx |
$0 |
$0 |
$4,001 |
$4,124 |
$5,978 |
$6,160 |
$9,979 |
$10,284 |
|
|
|
($3,916-$4,086) |
($1,650-$6,598) |
($5,851-$6,132) |
($2,464-$9,856) |
($9,768-$10,191) |
($4,114-$16,454) |
|
|
Εναλλακτικό μοντέλο |
|
|
|
|
|
|
|
|
|
AA |
$393 |
$366 |
$2,360 |
$2,199 |
$3,525 |
$3,285 |
$6,278 |
$5,851 |
|
($388-$397) |
($229-$549) |
($2,330-$2,383) |
($1,374-$3,299) |
($3,490-$3,560) |
($2,053-$4,928) |
($6,215-$6,340) |
($3,657-$8,776) |
|
|
AAwd |
$0 |
$0 |
$1,202 |
$1,100 |
$1,796 |
$1,643 |
$2,998 |
$2,742 |
|
|
|
($1,193-$1,212) |
($0,824-$1,650) |
($1,781-$1,810) |
($1,232-$2,464) |
($2,973-$3,022) |
($2,057-$4,113) |
|
|
Abiraterone |
$54,219 |
$51,114 |
$5,540 |
$5,224 |
$8,277 |
$7,802 |
$68,037 |
$64,140 |
|
($53,503-$54,936) |
($24,212-$94,158) |
($5,467-$5,614) |
($2,474-$9,621) |
($8,167-$8,386) |
($3,696-$14,374) |
($67,137-$68,937) |
($30,383-$118,153) |
|
|
Docetaxel |
$4,792 |
$4,772 |
$1,932 |
$1,924 |
$2,887 |
$2,875 |
$9,610 |
$9,571 |
|
($4,745-$6,203) |
($4,772-$5,454) |
($1,913-$1,951) |
($1,924-$2,199) |
($2,859-$2,915) |
($2,875-$3,285) |
($9,517-$9,704) |
($9,571-$10,939) |
|
|
Cabazitaxel |
$38,322 |
$33,638 |
$1,565 |
$1,374 |
$2,339 |
$2,053 |
$42,228 |
$37,065 |
|
($37,725-$38,918) |
($26,910-$47,093) |
($1,542-$1,590) |
($1,099-$1,924) |
($2,303-$2,376) |
($1,643-$2,874) |
($41,570-$42,884) |
($29,652-$51,892) |
|
|
OtherTx |
$0 |
$0 |
$4,134 |
$4,398 |
$6,176 |
$6,571 |
$10,309 |
$10,969 |
|
|
|
($4,045-$4,223) |
($1,924-$6,598) |
($6,043-$6,308) |
($2,874-9,856) |
($10,088-$10,531) |
($4,799-$16,454) |
|
Συντομογραφίες: 95% CI 95%
διάστημα εμπιστοσύνης, IQR Διατεταρτημοριακό
εύρος , ΑΑ αντιανδρογόνο, AAwd Απόσυρση αντιανδρογόνου, OtherTx Άλλες
θεραπείες.
⁕υποθέτοντας ότι μόνο το 95% των ασθενών έχουν λάβει φάρμακα για ιατρικό
ευνουχισμό· ⁕⁕ υποθέτοντας ότι μόνο
το 90% των ασθενών έχουν υποβληθεί σε θεραπεία με στόχο τα οστά.
Πηγή: Alice Dragomir, Daniela Dinea, [...], and Armen G Aprikian
Συνολικό κόστος
φαρμάκων κατά την περίοδο mCRPC
Πίνακας 15:Συνολικό και μηνιαίο κόστος φαρμάκων του mCRPC ανά τύπο φαρμάκου
|
|
Συνολικό κόστος
του για mCRPC ανά ασθενή |
Μηνιαίο κόστος για mCRPC ανά ασθενή |
Συνολικό κόστος
για mCRPC στον Καναδά |
||
|
Τρέχον μοντέλο |
Μέση τιμή
(95%CI) |
Διάμεση τιμή
(IQR) |
Μέση τιμή
(95%CI) |
(ετήσια ομάδα 4,000 mCRPCασθενών) |
|
|
Τύπος φαρμάκου: |
|
|
|
|
|
|
Πρωτογενής φαρμακευτική αγωγή⁕ |
$18,521
($18,126-$18,917) |
$10,386
($732-$32,411) |
$659 ($645-$688) |
$74,084,000 |
49.1% |
|
Φάρμακα για ιατρικό ευνουχισμό † |
$7,720
($7,628-$7,812) |
$6,873($3,849-$10,996) |
$274 ($271-$278) |
$30,882,000 |
20.4% |
|
Θεραπεία με στόχο τα οστά ‡ |
$11,532
($11,393-$11,671) |
$10,267
($5,749-$16,427) |
$410 ($405-$415) |
$46,045,000 |
30.5% |
|
Συνολικό κόστος του mCRPC |
$37,774
($37,147-$38,401) |
$27,526
($10,330-$59,835) |
$1,344
($1,322-$1,367) |
$151,011,000 |
100.0% |
|
Εναλλακτικό μοντέλο |
|
|
|
|
|
|
Τύπος φαρμάκου: |
|
|
|
|
|
|
Πρωτογενής φαρμακευτική αγωγή ** |
$55,616 ($54,620-$56,612) |
$48,996 ($732-$96,331) |
$1,491 ($1,464-$1,518) |
$222,462,000 |
68.5% |
|
Φάρμακα για ιατρικό ευνουχισμό † |
$10,249 ($10,117-$10.381) |
$9,347 ($4,398-$15,395) |
$274 ($271-$278) |
$40,997,000 |
12.6% |
|
Θεραπεία με στόχο τα οστά ‡ |
$15,311 ($15,113-$15,508) |
$13,963 ($6,571-$22,998) |
$410 ($405-$415) |
$61,242,000 |
18.9% |
|
Συνολικό κόστος του mCRPC |
$81,175 ($79,851-$82,501) |
$72,306 ($11,702-$134,723) |
$2,176 ($2,141-$2,211) |
$324,702,000 |
100.0% |
Συντομογραφίες: 95% CI 95% διάστημα εμπιστοσύνης, IQR Διατεταρτημοριακό εύρος
⁕περιλαμβάνει AA, docetaxel και abitarerone;
**περιλαμβάνει AA, abitarerone, docetaxel και cabazitaxel;
†υποθέτονταςότιμόνοτο 95% ασθενών έχει λάβει φαρμακευτική αγωγή για
ιατρικό ευνουχισμό
‡υποθέτοντας ότιμόνοτο90% των
ασθενών έχει υποβληθεί σε θεραπεία με στόχο τα οστά
Πηγή: Alice
Dragomir, Daniela Dinea, [...], and Armen G Aprikian
Ανάλυση ευαισθησίας: Τα αποτελέσματα
της ανάλυσης ευαισθησίας παρουσιάζονται στον Πίνακα 6(σημείωση: πάτησε στο 6 εδώ αν θέλεις να
τον δεις αλλά να ξέρεις ότι είναι σε καναδικά δολάρια).Δοκιμάστηκαν διάφορα σενάρια και τα
αποτελέσματα ήταν σύμφωνα με τα πρωταρχικά αποτελέσματα, εκτός από τα σενάρια
στα οποία η είσοδος στη φάση mCRPC αντιστοιχούσε με τη χορήγηση docetaxel
(τρέχον μοντέλο) και abiraterone (εναλλακτικό μοντέλο) για το 50%, 70% και 100%
των ασθενών, αντίστοιχα. Σε αυτά τα σενάρια, το μέσο κόστος ανά ασθενή ανά μήνα
αυξήθηκε στα $390 στο τρέχον μοντέλο και μέχρι τα $780 στο εναλλακτικό μοντέλο
.»52
Συμπεράσματα μεθόδου:
«Συζήτηση:
Άλλες
ενθαρρυντικές εξελίξεις στη θεραπεία του mCRPC αποκαλύφθηκαν πρόσφατα. Αυτές περιλαμβάνουν φάρμακα
όπως το TAK-700 (orteronel), ένα μη στεροειδή επιλεκτικό αναστολέα της
δραστικότητας 17,20-λυάσης του CYP17A - ένα βασικό ένζυμο στην παραγωγή
στεροειδών ορμονών καθώς και ραδιούχο
-223 διχλωριούχο (radium-223), ένα στοχευόμενο άλφα εκπομπό που συνδέεται
επιλεκτικά σε περιοχές αυξημένου οστικού μετασχηματισμού στις οστικές μεταστάσεις. Επιπλέον, η Αμερικανική Υπηρεσία Τροφίμων
και Φαρμάκων έχει εγκρίνει μια ανοσολογική θεραπεία, που ονομάζεται
sipuleucel-T για ασθενείς με μεταστατική νόσο και ελάχιστα συμπτώματα. Άλλες
θεραπείες που σχετίζονται κυρίως με την αντι-αγγειογένεση θα μπορούσαν
ενδεχομένως να είναι μέρος του φάσματος της θεραπείας τουmCRPC. Έτσι, είναι
πιθανό ότι μετά από μια σύντομη χρονική περίοδο, η διαχείριση του mCRPC θα
γίνει ακόμη πιο περίπλοκη και τα σχετικά φάρμακα θα κοστίζουν ακόμη υψηλότερα.
Είναι σαφές ότι υπάρχει έλλειψη γνώσης που
να εξετάζει το σύγχρονο κόστος της διαχείρισης του PCa, ιδιαίτερα στα
προχωρημένα στάδια. Η μελέτη μας βοηθάει να αποδειχθεί το κόστος που συνδέεται
με διάφορες ειδικές στρατηγικές διαχείρισης mCRPC. Ελπίζουμε ότι αυτές οι
πληροφορίες θα στηρίξουν τους υπεύθυνους για τη λήψη αποφάσεων στη διαδικασία
αξιολόγησης των νέων φαρμάκων, ενσωματώνοντας την οικονομική αξιολόγηση της
συνολικής διαχείρισης της νόσου στην παραδοσιακή ακολουθιακή γραμμή θεραπείας.
Επιπλέον, αυτό θα βοηθήσει τους κλινικούς γιατρούς να έχουν μεγαλύτερη επίγνωση
του οικονομικού αντίκτυπου των ιατρικών αποφάσεων τους. Δεν υπάρχει καμία
αμφιβολία ότι, προκειμένου να υπάρξουν νέες δαπανηρές θεραπείες, πρέπει να
βρεθεί εξοικονόμηση κόστους σε άλλα σημεία της διαδικασίας διαχείρισης της
νόσου. Για παράδειγμα, ο συνεχής ιατρικός ευνουχισμός κατά τη διάρκεια του
σταδίου mCRPC συνδέεται με σημαντικό κόστος, αλλά αμφισβητήσιμο όφελος. Το
κόστος νέων και δαπανηρών θεραπειών για το mCRPC μπορεί να
ανακτηθεί/αναπληρωθεί εν μέρει με τη μειωμένη χρήση θεραπειών LHRHa, που
εκτιμάται ότι αντιπροσωπεύουν το 21% του συνολικού κόστους του mCRPC.
Συντομογραφίες: PCa: Καρκίνος του
προστάτη; mCRPC: Μεταστατικός ανθεκτικός στον
ευνουχισμό καρκίνος του προστάτη; HT: Ορμονοθεραπεία; LHRHa: Αγωνιστές απελευθέρωσης ορμόνης ωχρινοτρόπου; PSA: Ειδικό αντιγόνο προστάτη; CRPC: Ευνουχοάντοχος καρκίνος
του προστάτη; ADT: Θεραπεία στέρησης ανδρογόνου / αφαίρεση
ανδρογόνων; AA: Αντιανδρογόνο; AAwd: Στέρηση αντιανδρογόνων;
OtherTx: Άλλες
θεραπείες; 95%CI: 95%
διάστημα εμπιστοσύνης; IQR: Ενδοτεταρτημοριακό εύρος»45
«Το κατώφλι στη σχέση κόστους στη σχέση
κόστους αποτελεσματικότητας, ερμηνεύεται ως ένας δείκτης με αριθμητή το
χρηματικό κόστος σε εθνικό νόμισμα και με παρονομαστή το όφελος υγείας σε μια
αντίστοιχη μονάδα μέτρησης».4
Σύμφωνα με το αυστηρό κατώφλι ο δείκτης QALYsείναι καθοριστικό κριτήριο για τη διάχυση
των πόρων ενώ το ελαστικό ενσωματώνει και άλλες παραμέτρους προκειμένου να αποφασιστεί η αποδοχή του
προγράμματος».4«Σύμφωνα με τον μελετητή Drummondτα κλινικά αποτελέσματα θα συνοδεύουν τις αναλύσεις κόστους –
αποτελεσματικότητας για την υγεία πριν ληφθεί απόφαση για την κατανομή των
πόρων ενώ η τιμή κατώφλι θα καθιερωθεί στις αναλύσεις κόστους
αποτελεσματικότητας για την υγεία»4
«Για την κατηγορία του μεταστατικού
καρκίνου του προστάτη η κυριαρχούσα θεραπεία είναι η χειρουργική αντιμετώπιση
με ασφαλή αποτελέσματα. Αντίθετα με την ανοσοθεραπεία «που αποτελεί ένα από τα
πιο σύγχρονα εργαλεία , που διαθέτει η επιστημονική κοινότητα έναντι των
νεοπλασιών , η κατανόηση των μηχανισμών και των σηματοδοτικών μονοπατιών που
βρίσκονται πίσω από το κατασταλμένο ανοσοποιητικό σύστημα του οργανισμού, κατά
τη διάρκεια του καρκίνου, έχει ήδη ξεκινήσει και αναμένεται
να κορυφωθεί μέσα στα επόμενα
χρόνια (4).
Ο συνδυασμός των 2 χημειοθεραπευτικών
προσεγγίσεων της Μετρονομικής χημειοθεραπείας και της χημειοθεραπείας, μπορεί
να διευρύνει το φάσμα των εφαρμογών των αντικαρκινικών φαρμάκων, αυξάνοντας
παράλληλα την αποτελεσματικότητα της θεραπείας. Συνδυασμός των δύο ανωτέρω
μεθόδων δείχνει ενίσχυση της αποτελεσματικότητας της ανοσοθεραπείας και
ανοίγοντας το δρόμο για το σχεδιασμό και την έγκριση φαρμακευτικών αγωγών με
αυξημένη και παρατεταμένη αποτελεσματικότητα αλλά με μειωμένη τοξικότητα.
Παρόλα αυτά η θέση της Μετρονομικής χημειοθεραπείας
από μόνη της ή σε συνδυασμό με την ανοσοθεραπεία στην καταπολέμηση του
καρκίνου, πρέπει να διερευνηθεί περαιτέρω». Συνδυασμός μετρονομικής
χημειοθεραπείας και ανοσοθεραπείας – θεωρητική και πειραματική προσέγγιση»12
«Την
ποιότητα της οικονομικής ανάλυσης για τη λήψη απόφασης την καθορίζουν
και άλλοι παράγοντες»3, όπως :
6. «Η ανάγκη
για περίθαλψη με βάση την ιατρική απόδειξη που απορρέει κυρίως από τη
δυσανάλογη αύξηση των υγειονομικών αναγκών σε σχέση με την αύξηση των
διαθέσιμων πόρων».3
7. Η γήρανση
του πληθυσμού, η εισροή νέων τεχνολογιών , οι αυξανόμενες προσδοκίες των
ασθενών και οι αυξανόμενες προσδοκίες των επαγγελματιών υγείας3
8. «Στον
συνδυασμό εισροών που επιτυγχάνουν το μέγιστο αποτέλεσμα με δεδομένο το κόστος
παραγωγής (αρχή της διανεμητικής αποτελεσματικότητας)
9. Το
αναθεωρημένο πλαίσιο από τους Labelleet.al. ανάλυσης της δυνατότητας των γιατρών να προκαλούν
ζήτηση για τις υπηρεσίες τους προκλητή ζήτηση υπηρεσιών υγείας»49
10. «Ο
έλεγχος του κόστους και ποιότητας μέσω της ακριβούς κοστολόγησης (συλλογή δεδομένων
κλινικών και οικονομικών ως ενδεδειγμένη κλινική διαδρομή (κλινικά πρωτόκολλα,
ενσωμάτωση καινοτομίας, συνευθύνη ιατρών)»7DRGspatienthealthcare
«Δεδομένου ότι στην οικονομική αξιολόγηση σκοπός δεν είναι
η ελαχιστοποίηση του κόστους, όσο η μείωση του ρυθμού αύξησης των
υπέρογκων δαπανών και φυσικά η ορθολογική χρήση των διαθέσιμων πόρων, εδώ το
κοινωνικό κόστους συνυπολογίζεται στην λήψη απόφασης και τα κριτήρια της
οικονομικής αξιολόγησης ενσωματώνουν τις απαιτήσεις για κοινωνική ευημερία». Μελέτη
κόστους – χρησιμότητας σε ασθενείς που έχουν υποβληθεί σε τοποθέτηση οδοντικών
εμφυτευμάτων».10
«Η περίοδος ανάκτησης που είναι ένας χρυσός κανόνας που υποστηρίζει την
αποδοχή ενός επενδυτικού έργου, εφόσον αυτό επιστρέφει τις εκροές του μέσα σε
μια προκαθορισμένη χρονική περίοδο , η οποία μπορεί να προσαρμοστεί ώστε να
περιλάβει διάφορα στοιχεία , όπως το αρχικό κόστος επενδύσεων ή το κόστος συν ένα αποδεκτό
περιθώριο κέρδους.
Επειδή επιλέγεται ως μέθοδος προσέγγισης στην αρχική εξέταση της
επενδυτικής πρότασης Όμως δεν διατίθεται ο μηχανισμός για να εξεταστούν τα
πιθανά έσοδα από μια επένδυση μετά το τέλος της περιόδου ανάκτησης και συνεπώς
τα αντιμετωπίζει ως απρόβλεπτα έσοδα.»53
«Οι σημαντικές αποφάσεις που πρέπει να ληφθούν στο πλαίσιο ενός οργανωμένου
συστήματος υγείας αφορούν
§ κάλυψη (αποζημίωση του κόστους μιας
υγειονομικής παρέμβασης)» εδώ θεραπευτικής,
§ Στην
ορθολογική και αποδοτική κατανομή των σπάνιων πόρων .Ένα κατάλληλο εργαλείο για ορθολογική
κατανομή των πόρων είναι η οικονομική αξιολόγηση η οποία γίνεται με σκοπό να
αποδείξει αν οι εξεταζόμενες θεραπευτικές προσεγγίσεις δεν σπαταλούν πόρους
υγείας»6 Στην τελική απόφαση υπεισέρχονται και κοινωνικά και
κριτήρια αξίας.
§ «Σε κάποιες
χώρες προαπαιτείται πριν την αποζημίωση οικονομική αξιολόγηση των
παρεμβάσεων.
§ Η ανάλυση
που προηγήθηκε, «προσδιόρισε στην ουσία την αποδοτικότητα της παρέμβασης και
αποτελεί τη σχέση κόστους ευκαιρίας, όπου το κόστος είναι η νομισματική αξία
των χρησιμοποιούμενων εισροών για την πραγματοποίηση μιας διαδικασίας και το
,όφελος όσο και τα αποτελέσματα είναι οι εκροές. Δεδομένης της οικονομικής
ύφεσης που διανύει η χώρα μας τα τελευταία χρόνια, αλλά και των
μνημονιακών υποχρεώσεων που επιβάλλουν
συνεχή περιστολή και των δαπανών για την υγεία, κρίνονται επιβεβλημένες οι
οικονομικές αξιολογήσεις των θεραπευτικών παρεμβάσεων προκειμένου να
επιλέγονται εκείνες που θα μεγιστοποιούν τα οφέλη για τον ασθενή με το λιγότερο
δυνατό κόστος για τον υγειονομικό τομέα.»7
«Συμπεράσματα: Στην ανάλυση CEA «η μέτρηση της αποτελεσματικότητας είναι σε
κερδισμένα έτη ζωής . Το μεγάλο πλεονέκτημα είναι ότι η ανθρώπινη ζωή και τα
υγειονομικά αποτελέσματα δεν αποτιμώνται
σε χρήμα, ενώ μόνο συστήματα, τεχνολογίες, προγράμματα ή υπηρεσίες με κοινές
μονάδες εκροών μπορούν να συγκριθούν.
Στη συγκεκριμένη μελέτη του Υ.Υ. επειδή «η οικονομική αξιολόγηση αφορά
την επίτευξη ή όχι του στόχου της μεγιστοποίησης των βελτιώσεων στην υγεία που
παράγονται με ένα δεδομένο επίπεδο δημόσιας δαπάνης , η κοινωνική δικαιοσύνη
αφορά τη δίκαιη κατανομή των βελτιώσεων
αυτών στο σύνολο του πληθυσμού « 5ενδεδειγμένη είναι η ανάλυση του
κόστους αποτελεσματικότητας συγκριτικά ανάμεσα στις δύο θεραπείες, καθόσον «η οικονομική αξιολόγηση
κατευθύνει τη λήψη αποφάσεων κατανομής πόρων μέσα στα πλαίσια καθορισμένων προϋπολογισμών,
σε εκείνες τις επιλογές που προσφέρουν τα μέγιστα δυνατά αποτελέσματα»1
Στις
περισσότερες περιπτώσεις υπάρχουν διαφορές «στην ασφάλεια, αποτελεσματικότητα,
την τοξικότητα και την οικονομία των διάφορων εναλλακτικών θεραπευτικών
επιλογών για τους ασθενείς με καρκίνο»1
Το ίδιο
συμβαίνει και δύο αυτές συγκριτικές
αξιολογήσεις.
Τα αδύνατα σημεία είναι ότι « ο προϋπολογισμός της θεραπευτικής
παρέμβασης είναι προσανατολισμένος στην πλευρά των εκροών και όχι των εισροών.
Από την άλλη η οριακή ανάλυση ,
προσπαθεί να εξετάσει το ενδεχόμενο μεταβολών στη χρήση των πόρων μεταξύ
προγραμμάτων υγείας με απώτερο σκοπό τη βελτίωση της κοινωνικής ευημερίας. Αυτή
συνίσταται στην εξέταση του αν μια μετατόπιση οικονομικών πόρων κάποιου
συγκεκριμένου ποσού από ένα πρόγραμμα υγείας σε κάποιο άλλο , επιφέρει αύξηση
του συνολικού οφέλους , δεδομένων των συνολικών διατιθέμενων πόρων.4
βέβαια οι δύο δημόσιες θεραπείες
οφείλουν να δύνανται να κρίνουν και την αξία που προκύπτει εντός
της μακρόχρονης αποτελέσματος του
ατομικού συμφέροντος .
«Επειδή οι προϋπολογισμοί για την
υγειονομική Περίθαλψη είναι
περιορισμένοι , μπορεί να καθοδηγήσει και να βοηθήσει τους υπεύθυνους για τη
λήψη αποφάσεων να μεγιστοποιήσουν την αξία των χρημάτων που δαπανώνται, δηλαδή
τα χρόνια ζωής που κερδίζονται ανά ευρώ». Το ζήτημα αυτό καθίσταται ακόμη πιο
σημαντικό όταν κάποιος πρέπει να εξετάσει αν προσθέσει ένα ακριβό παράγοντα –
θεραπεία πάνω από έναν άλλο , για να βοηθήσει τους ασθενείς να επιβιώσουν για
ένα ή δύο ακόμη μήνες κατά μέσο όρο».5 Αυτό προκύπτει και στις 2
θεραπείες του καρκίνου του προστάτη.
Το θέμα είναι «αν αξίζει τα επιπλέον χρήματα»1
«Έτσι με γνώμονα την οικονομική δυσπραγία που υφίσταται στην χώρα μας ,
αλλά και των δυνατοτήτων της ενόψει του μεσοπρόθεσμου , που μειώνουν αυξητικά
τα έξοδα στο χώρο της υγείας, καθίσταται αναγκαίο οι συγκριτικές αξιολογήσεις
των θεραπευτικών προσεγγίσεων να διαλέγουν εκείνες που θα αυξάνουν τα οφέλη για
τους αρρώστους με το χαμηλότερο εφικτό κόστος για τον χώρο της δημόσιας υγείας στην χώρα μας».1
«Καθόσον στις περισσότερες χώρες γίνεται μια προσπάθεια, να γίνονται
οικονομικές αναλύσεις κόστους αποτελέσματος πριν υιοθετηθεί μια καινούργια
ιατρική πρακτική, οι πρωτοβουλίες κάποιων συστημάτων υγείας έχει εκφραστεί με
την έκδοση οικονομικών οδηγιών με τις κλινικές οδηγίες. Είναι 1 σημαντικό βήμα
που θα φέρει θετικές επιδράσεις στην οικονομική αποδοτικότητα. Οι οικονομικές
οδηγίες θα πρέπει να αναθεωρούνται συχνά
ανάλογα με τις μεταβολές στους τομείς της αγοράς, τις υγειονομικές ανάγκες, τα
κλινικά δεδομένα και στην παραγωγικότητα».4
![]()
Συμπεράσματα
«Συμπερασματικά, σε μια μέση περίοδο
μικρότερη των τριών ετών, δείξαμε ότι το κόστος των φαρμάκων mCRPC είναι
σημαντικό και ευάλωτο στην αύξηση στο εγγύς μέλλον σε απαγορευτικά επίπεδα. Στο
σημερινό πλαίσιο της αυξανόμενης θεραπείας και του κόστους των φαρμάκων, ειδικά
για τη θεραπεία των προχωρημένων καρκίνων, η οικονομική επιβάρυνση για το
καναδικό σύστημα υγείας και για τους Καναδούς έχει αυξηθεί δραματικά. Ως εκ
τούτου, η πρόσβαση σε φάρμακα για τον καρκίνο για το mCRPC στο καναδικό σύστημα
υγείας έχει γίνει πρόκληση. Με το μοντέλο μας, μπορούμε να προσομοιώσουμε τη
διαχείριση του mCRPC και τις σχετικές δαπάνες του κατά τη διάρκεια αυτής της
περιόδου. Αυτό μπορεί να αποτελέσει ένα πολύτιμο εργαλείο για τους υπεύθυνους
για τη λήψη αποφάσεων και για τους ηγέτες των κλινικών, βοηθώντας τους να
επηρεάσουν τις αποφάσεις σχετικά με την πρόσβαση του κοινού σε καινοτόμες
θεραπείες και βοηθώντας στην επίτευξη βέλτιστης διαχείρισης για αυτούς τους ασθενείς.
Επιπλέον, αυτό το μοντέλο είναι σε θέση να παρέχει μια εκτίμηση σε πραγματικό
χρόνο του οικονομικού αντίκτυπου στο συνολικό κόστος του mCRPC μιας
συγκεκριμένης απόφασης σε ένα συγκεκριμένο επίπεδο κατά τη διάρκεια της
θεραπείας του mCRPC.»52
![]()
Βιβλιογραφία
1.
ΒΟΥΛΓΑΡΗ Ι.«Ανάλυση κόστους - αποτελεσματικότητας
του Nivolumab έναντι του Docetaxel σε προχωρημένο Πλακώδη Μη Μικροκυτταρικό Καρκίνο του Πνεύμονα» .ΤΜΗΜΑ
ΟΙΚΟΝΟΜΙΚΗΣ ΕΠΙΣΤΗΜΗΣ :ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΕΙΡΑΙΩΣ Πειραιάς 2017
ΠΡΟΓΡΑΜΜΑΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΟΙΚΟΝΟΜΙΚΑ & ΔΙΟΙΚΗΣΗ ΤΗΣ ΥΓΕΙΑΣ».
2.
B. Alemayehu,
E.Buysman, D.Parry,L. Becker &F.Nathan Pages 351-361 |Published onlineQ24
May 2010
3.
Πρασιάδης Χ.ΚΑΡΚΙΝΟΣ ΤΟΥ ΠΡΟΣΤΑΤΗ. ΣΧΟΛΗ
ΕΠΑΓΓΕΛΜΑΤΩΝ ΥΓΕΙΑΣ ΚΑΙ ΠΡΟΝΟΙΑΣ: Τ.Ε.Ι. ΑΝΑΤΟΛΙΚΗΣ ΜΑΚΕΔΟΝΙΑΣ ΚΑΙ ΘΡΑΚΗΣ ΔΕΚΕΜΒΡΙΟΣ 2014 ΣΧΟΛΗ ΕΠΑΓΓΕΛΜΑΤΩΝ ΥΓΕΙΑΣ ΚΑΙ ΠΡΟΝΟΙΑΣ ΤΜΗΜΑ
ΝΟΣΗΛΕΥΤΙΚΗΣ
4.
Μίτσουλη Ε.
Οικονομική Αξιολόγηση
Εναλλακτικών Θεραπειών – Κατανομή Πόρων. ΙΕ
ΕΚΠΑΙΔΕΥΤΙΚΗ ΣΕΙΡΑ ΤΜΗΜΑ ΚΟΙΝΩΝΙΚΗΣ ΔΙΟΙΚΗΣΗΣ ΠΡΟΓΡΑΜΜΑ ΔΙΟΙΚΗΣΗΣ
ΥΠΗΡΕΣΙΩΝ ΥΓΕΙΑΣ ΤΕΛΙΚΗ ΕΡΓΑΣΙΑ :Εθνική Σχολή Δημόσιας Διοίκησης ΑΘΗΝΑ,
ΟΚΤΩΒΡΙΟΣ 2004
5.
European
Association of Urology (eau), https://eau18.uroweb.org/
6.
Πουλάκης από τον δικτυακό τόπο http://www.poulakis-urology.com/da-vinci-ourologikes-epembaseis
7.
Μπαλασοπούλου σύγχρονες πολιτικές ελέγχου και
συγκράτησης του κόστους των υπηρεσιών υγείας Κοστολόγηση και Τιμολόγηση
8.
Αθανασιάδη Ε. Ανάλυση κόστους - αποτελεσματικότητας
εναλλακτικών πολιτικών για τον προσυμπτωματικό έλεγχο του καρκίνου του τραχήλου
της μήτρας. ΤΜΗΜΑ ΟΙΚΟΝΟΜΙΚΗΣ ΕΠΙΣΤΗΜΗΣ : ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΕΙΡΑΙΩΣ Πειραιάς 2015
9.
Γ.Ν. Υφαντόπουλος Τα Οικονομικά της Υγείας
10.
Παππά Ε.
«Μελέτη κόστους- χρησιμότητας σε ασθενείς που έχουν υποβληθεί σε
τοποθέτηση οδοντικών εμφυτευμάτων . Τμήμα Επιστημών Υγείας: Εuropean University Cyprus Αθήνα, Φεβρουάριος 2017 ‘’Πρόγραμμα
Μεταπτυχιακών Σπουδών Διοίκηση Μονάδων Υγείας»
11.
Albertsen, P.C.
Observational studies and the natural history of screen-detected prostate cancer.
CurrOpinUrol, 2015. 25: 232.
12. Bruinsma, S.M., et al. Expert consensus document: Semantics
in active surveillance for men with localized prostate cancer - results of a
modified Delphi consensus procedure. Nat Rev Urol, 2017. 14: 312.
13. Adolfsson, J. Watchful waiting and
active surveillance: the current position. BJU Int, 2008. 102: 10.
14. Carter, H.B., et al. Expectant management of prostate
cancer with curative intent: an update of the Johns Hopkins experience. J Urol,
2007. 178: 2359.
15. Chodak, G.W., et al. Results of conservative management
of clinically localized prostate cancer. N Engl J Med, 1994. 330: 242.
16.
Yaxley, J.W., etal.
Robot-assisted laparoscopic prostatectomy versus open radical retropubic
prostatectomy: early outcomes from a randomised controlled phase 3 study.
Lancet, 2016. 388: 1057
17.
Adolfsson, J., et
al. The 20-Yr outcome in patients with well- or moderately differentiated
clinically localized prostate cancer diagnosed in the pre-PSA era: the
prognostic value of tumour ploidy and comorbidity. Eur Urol, 2007. 52: 1028.
18.
Hayes, J.H., et al. Observation versus initial treatment for men with
localized, low-risk prostate cancer: a cost-effectiveness analysis. Ann Intern
Med, 2013. 158: 853.
19.
Albertsen, P.C., et
al. Competing risk analysis of men aged 55 to 74
years at diagnosis managed conservatively for clinically localized prostate
cancer. Jama, 1998. 280: 975.
20. Iversen, P., et al. Bicalutamide (150 mg) versus
placebo as immediate therapy alone or as adjuvant to therapy with curative
intent for early nonmetastatic prostate cancer: 5.3-year median followup from
the Scandinavian Prostate Cancer Group Study Number 6. J Urol, 2004. 172: 1871.
21. Ash, D., et al. ESTRO/EAU/EORTC recommendations on
permanent seed implantation for localized prostate cancer. Radiother Oncol,
2000. 57: 315.
22. Martens, C., et al. Relationship of the
International Prostate Symptom score with urinary flow studies, and
catheterization rates following 125I prostate brachytherapy. Brachytherapy,
2006. 5: 9.
23.
Pagliarulo, V., et al.
Contemporary role of androgen deprivation
therapy for prostate cancer. EurUrol, 2012. 61: 11.
24.
Fizazi, K., etal.
Abiraterone plus Prednisone in Metastatic, Castration-Sensitive Prostate
Cancer. N Engl J Med, 2017. 377: 352.
25.
James, N.D., et al. Abiraterone for Prostate Cancer Not Previously
Treated with Hormone Therapy. N Engl J Med, 2017. 377: 338.
26.
Sweeney, C.J.,
etal. Chemohormonal Therapy in Metastatic Hormone-Sensitive Prostate Cancer. N
Engl J Med, 2015. 373: 737.
27.
James, N.D., et al. Addition of docetaxel, zoledronic acid, or both to
first-line long-term hormone therapy in prostate cancer (STAMPEDE): survival
results from an adaptive, multiarm, multistage, platform randomised controlled
trial. Lancet, 2016. 387: 1163.
28. Gravis, G., et al. Androgen-deprivation therapy
alone or with docetaxel in non-castrate metastatic prostate cancer (GETUG-AFU
15): a randomised, open-label, phase 3 trial. LancetOncol, 2013. 14: 149.
29.
Eisenhauer, E.A., et
al. New response evaluation criteria in solid
tumours: revised RECIST guideline (version 1.1). Eur J Cancer, 2009. 45: 228.
30.
Ryan, C.J., etal.
Abiraterone in metastatic prostate cancer without previous chemotherapy. N Engl
J Med, 2013. 368: 138.
31.
Ryan, C.J., et al. Abiraterone acetate plus prednisone versus placebo
plus prednisone in chemotherapy-naive men with metastatic castration-resistant
prostate cancer (COU-AA-302): final overall survival analysis of a randomised,
double-blind, placebo-controlled phase 3 study. Lancet Oncol, 2015. 16: 152.
32. Beer, T.M., et al. Enzalutamide in
metastatic prostate cancer before chemotherapy. N Engl J Med, 2014. 371: 424.
33.
Graff, J.N., et al. Efficacy and safety of enzalutamide in patients 75
years or older with chemotherapy-naive metastatic castration-resistant prostate
cancer: results from PREVAIL. Ann Oncol, 2016. 27: 286.
34.
Evans, C.P., et al. The PREVAIL Study: Primary Outcomes by Site and
Extent of Baseline Disease for Enzalutamide-treated Men with Chemotherapy-naive
Metastatic Castration-resistant Prostate Cancer. Eur Urol, 2016. 70: 675.
35.
annock, I.F., et al. Docetaxel plus prednisone or mitoxantrone plus
prednisone for advanced prostate cancer. N Engl J Med, 2004. 351: 1502.
36.
Scher, H.I., et al. Trial Design and Objectives for
Castration-Resistant Prostate Cancer: Updated Recommendations From the Prostate
Cancer Clinical Trials Working Group 3. J Clin Oncol, 2016. 34: 1402.
37. Smith, M.R., etal. Disease and host characteristics
as predictors of time to first bone metastasis and death in men with
progressive castration-resistant nonmetastatic prostate cancer. Cancer, 2011. 117:
2077.
38. de Bono, J.S., et al. Prednisone plus
cabazitaxel or mitoxantrone for metastatic castration-resistant prostate cancer
progressing after docetaxel treatment: a randomised open-label trial. Lancet,
2010. 376: 1147.
39. Parker, C., et al. Alpha emitter radium-223 and
survival in metastatic prostate cancer. N Engl J Med, 2013. 369: 213.
40. Saad, F., etal. A randomized, placebo-controlled
trial of zoledronic acid in patients with hormone-refractory metastatic
prostate carcinoma. J Natl Cancer Inst, 2002. 94: 1458.
41. Marco, R.A., et al. Functional and
oncological outcome of acetabular reconstruction for the treatment of
metastatic disease. J Bone Joint Surg Am, 2000. 82: 642.
42. Παπαδοπούλου,
Λ. Εξελίξεις στη Θεραπεία του Καρκίνου ΑΝΟΣΟΘΕΡΑΠΕΙΑ 3ο Πανελλήνιο
Συνέδριο Εφαρμοσμένης Φαρμακευτικής 6-7 Μαϊου 2017 Θεσσαλονίκη
43. Κύπρου
Μελέτη κόστους -αποτελεσματικότητας της
υποκάψιας ορχεκτομής σε σύγκριση με το φαρμακευτικό ορμονικό ευνουχισμό στο
μεταστατικό καρκίνο του προστάτη». Σούφης , Ε. 2015- 03 -20.
44. Bασικά Οικονομικά της Υγείας, Εργαλεία και Θεσμοί
Μέρος 1
45. Leslie S. Wilson, PhD, Ross Tesoro, PharmD, Eric P.
Elkin, MPH, Natalia Sadetsky, MD, MPH, Jeanette M. Broering, RN, MS, MPH, David
M. Latini, PhD, Janeen DuChane, PhD,
Reema R. Mody, MBA, PhD, Peter R. Carroll, MD, Cumulative Cost Pattern
Comparison of Prostate Cancer Treatments, PabMed, 21 December 2006
46.
Το μέσο κόστος της χημειοθεραπείας http://el.winesino.com/cancer/chemotherapy/1013026110.html
47.
Τρία νέα φάρμακα για τον Καρκίνο του Προστάτη https://www.organiclife.gr/el/health/756-cancer.html
48.
Τούντας Γ. , Οικονόμου Ν. « Αξιολόγηση των Υπηρεσιών Υγείας», Αρχεία Ελλ. Ιατρικής
2007, 24 (1)¨7-21 και «Η αξιολόγηση των ιατρικών παρεμβάσεων και η τεκμηριωμένη
φροντίδα υγείας», Αρχεία Ελλ. Ιατρικής 2007, 24 (1) : 22-33.
- HΛΙΑ E. «Συνδυασμός μετρονομικής χημειοθεραπείας και ανοσοθεραπείας -
θεωρητική και πειραματική προσέγγιση». ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ
ΙΑΤΡΙΚΗΣ :ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΙΩΑΝΝΙΝΑ 2017 . ΜΕΤΑΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ
«ΒΑΣΙΚΕΣ ΒΙΟΙΑΤΡΙΚΕΣ ΕΠΙΣΤΗΜΕΣ (ΒΒΕ) ΜΕΤΑΠΤΥΧΙΑΚΟ ΔΙΠΛΩΜΑ ΕΙΔΙΚΕΥΣΗΣ (ΜΔΕ)
- Μανιαδάκης
Ν. Υφαντόπουλος Γ (1996) Προκλητή Ζήτηση Υπηρεσιών Υγείας, Αρχεία, Ιαν
-Φεβ. 1996, τόμος 13, τεύχος1 σελ 58-68
- Σ. Αγγελάκη, (2015) «ΘΕΡΑΠΕΥΤΙΚΑ
ΠΡΩΤΟΚΟΛΛΑ ΧΟΡΗΓΗΣΗΣ ΧΗΜΕΙΟΘΕΡΑΠΕΥΤΙΚΩΝ ΦΑΡΜΑΚΩΝ ΣΕ ΑΣΘΕΝΕΙΣ ΜΕ
ΝΕΟΠΛΑΣΜΑΤΙΚΑ ΝΟΣΗΜΑΤΑ» στο Ογκολόγων Παθολόγων Ελλάδας (ΕΟΠΕ)Χ. Ανδρεάδης
(επιμ.) Εταιρεία, 6η έκδοση, Αθήνα, σελ 152-157
- Alice Dragomir, Daniela Dinea, [...], and
Armen G Aprikian
- Παράρτημα 5Α, Μερικά
εκλαϊκευμένα κριτήρια για τη μέτρηση της απόδοσης διαφόρων επενδυτικών σχεδίων
- B. Alemayehu, E.Buysman, D.Parry,L. Becker &F.Nathan Pages
351-361 |Published onlineQ24 May 2010
- Κιάκου ,Μ. Τόλια ,Μ.Τσουκαλάς Ν.
Aνοσοθεραπεία
του καρκίνου . Μια διαφορετική προσέγγιση στη θεραπεία της νεοπλασματικής
νόσου .ΑΡΧΕΙΑ ΕΛΛΗΝΙΚΗΣ ΙΑΤΡΙΚΗΣ 2015, 32 (4):461-466
- Παπουτσάκη Μ. Η επιλογή της θεραπείας με βάση τη σοβαρότητα της
ψωρίασης και το οικονομικό κόστος .Γ’ Δερματολογική Κλινική , Νοσοκομείο
Α. Συγγρός.
![]()
![]()
© Copyright-VIPAPHARM. All rights reserved

![]()